
Đề thi giữa HK2 môn Hóa học 12 năm 2021
Đề thi nằm trong bộ sưu tập: Tổng hợp đề thi trắc nghiệm ôn luyện Hóa học 12
Số câu hỏi: 40 câuSố mã đề: 1 đềThời gian: 1 giờ
110,649 lượt xem 8,508 lượt làm bài
Xem trước nội dung:
Cho 15,6 gam hỗn hợp X gồm Al và Al2O3 tác dụng hoàn toàn với dung dịch HCl dư, thu được 6,72 lít khí H2 (đktc). Tính phần trăm khối lượng mỗi chất có trong hỗn hợp X.
Nhiệt phân hoàn toàn muối X thu được kim loại và hỗn hợp khí. Muối X là
Hiđrocacbon nào sau đây không làm mất màu dung dịch brom ở nhiệt độ thường?
Thực hiện phản ứng hiđro hóa CH3CHO (xúc tác Ni, to) thu được sản phẩm hữu cơ nào sau đây?
Thủy phân este X có công thức phân tử C4H8O2 trong dung dịch NaOH đun nóng, sản phẩm thu được có chứa natri fomat. Số công thức cấu tạo thỏa mãn điều kiện của X là
Cho hình vẽ mô tả thí nghiệm điều chế khí Z từ dung dịch X và chất rắn Y:
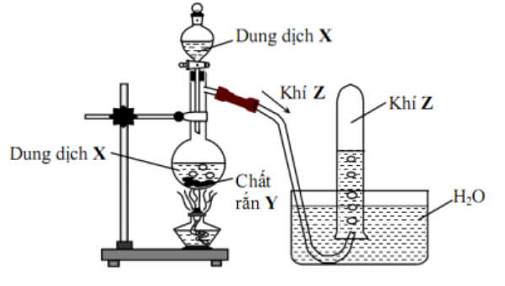
Khí Z được tạo ra từ phản ứng hóa học nào sau đây?
Kim loại có khối lượng riêng nhỏ nhất, là vật liệu quan trọng trong việc sản xuất anot của pin điện là
Phản ứng hóa học xảy ra trong quá trình tạo thạch nhũ trong các hang động đá vôi là
Quặng manhetit là loại quặng giàu sắt nhưng hiếm gặp trong tự nhiên. Thành phần chính của quặng manhetit là:
Thí nghiệm nào sau đây không xảy ra phản ứng hóa học?
Chất nào sau đây là chất điện li mạnh?
Amin X chứa vòng benzen có công thức phân tử: C6H7N. Danh pháp nào sau đây không phải của amin X?
Trong các dung dịch: HOOC-CH2-CH2-CH(NH2)-COOH (1); H2N-CH2-COOH (2);
C6H5-NH2 (anilin) (3); H2N-CH2-CH(NH2)-COOH (4), CH3-CH2-NH2 (5). Số dung dịch làm xanh quỳ tím là
Pentapeptit X mạch hở, được tạo nên từ một loại amino axit Y (trong Y chỉ chứa một nhóm amino và một nhóm cacboxyl). Phân tử khối của X là 513. Phân tử khối của Y là:
Cho các chất: Si, NH4NO3, Al, CO2, CO, H3PO4. Số chất phản ứng được với dung dịch NaOH loãng khi đun nóng là:
Chất nào không phải là polime:
Nhận định nào sau đây đúng?
Thủy phân hoàn toàn m gam metyl fomat bằng 74 ml dung dịch NaOH 1M dư, đun nóng. Cô cạn dung dịch sau phản ứng thu được 4,08 gam rắn khan. Giá trị của m là:
Nhúng một lá Zn vào 200 ml dung dịch CuSO4 nồng độ x (mol/l) đến khi dung dịch mất màu hoàn toàn thấy khối lượng lá Zn giảm 0,15 gam so với ban đầu (coi kim loại tạo thành bán hết vào lá kẽm). Giá trị của x là:
Glucozơ và xenlulozơ có cùng đặc điểm nào sau đây?
Hòa tan hoàn toàn m gam hỗn hợp Na và Ba vào nước thu được dung dịch X và 4,48 lít H2 (đktc). Để trung hòa X cần vừa đủ 400ml dung dịch H2SO4 xM. Giá trị của x là
Hòa tan hoàn toàn m gam hỗn hợp X gồm Al và Mg trong 500 ml dung dịch HNO3 1M thu được dung dịch Y và khí NO. Cho từ từ dung dịch NaOH vào dung dịch Y, lượng kết tủa tạo thành được biểu diễn theo đồ thị sau:
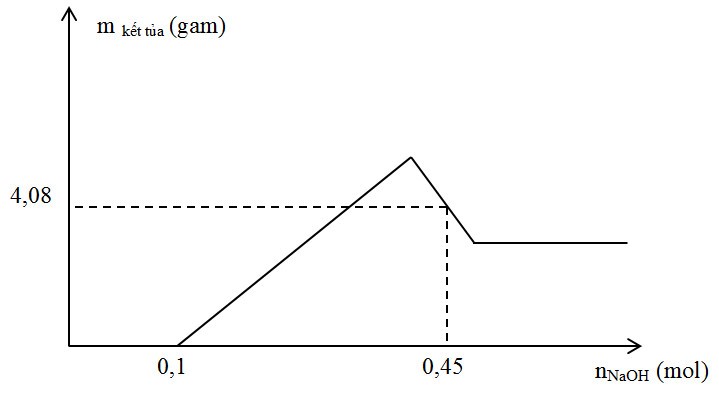
Giá trị của m là
Cho các phát biểu sau:
(a) Các kim loại Na, K, Ba đều phản ứng mạnh với nước.
(b) Kim loại Cu tác dụng được với dung dịch hỗn hợp NaNO3 và H2SO4 (loãng).
(c) Cho lá sắt vào dung dịch CuSO4 xảy ra hiện tượng ăn mòn điện hóa.
(d) Cho bột Cu vào lượng dư dung dịch FeCl3, thu được dung dịch chứa ba muối.
(e) Hỗn hợp Al2O3 và Na (tỉ lệ mol tương ứng 1:1) tan hoàn toàn trong nước dư.
(f) Lưu huỳnh, photpho, ancol etylic đều bốc cháy khi tiếp xúc với CrO3.
Số phát biểu đúng là
Cho sơ đồ phản ứng sau:
Biết Y, Z, T đều là hợp chất của crom. Các chất X, T lần lượt là:
Cho các phát biểu sau:
(1) Có thể phân biệt axit fomic và anđehit fomic bằng phản ứng với dung dịch AgNO3/NH3.
(2) Tất cả các peptit đều phản ứng với Cu(OH)2 tạo dung dịch màu tím.
(3) Amilozơ và amilopectin là đồng phân của nhau.
(4) Điều chế anđehit axetic trong công nghiệp bằng phản ứng oxi hóa etilen.
(5) Glucozơ và fructozơ đều làm mất màu dung dịch nước Br2.
(6) Tách H2O từ etanol dùng điều chế etilen trong công nghiệp.
Số phát biểu đúng là:
Cho sơ đồ biến hóa: X → Y → Z (muối)
Phát biểu nào sau đây không đúng:
Phát biểu nào sau đây không đúng?
Cho các dung dịch: CH3COOH, C2H4(OH)2, saccarozơ, C2H5OH; anbumin. Số dung dịch phản ứng được với Cu(OH)2 là
Hòa tan hoàn toàn m gam Cu trong dung dịch HNO3 dư thu được dung dịch X không chứa muối amoni và 4,48 lít hỗn hợp khí Y gồm NO và NO2 (đktc), tỉ khối của Y so với H2 là 17. Giá trị của m là
Trạng thái, nhiệt độ nóng chảy, nhiệt độ sôi và độ tan trong nước của ba chất hữu cơ X, Y, Z được trình bày trong bảng sau:
|
| Trạng thái (ở điều kiện thường) | Nhiệt độ sôi (oC) | Nhiệt độ nóng chảy (oC) | Độ tan trong nước (g/100 ml) | |
| 20oC | 90oC | ||||
| X | Rắn | 181,7 | 43 | 8,3 | ∞ |
| Y | Lỏng | 184,1 | -6,3 | 3,0 | 6,4 |
| Z | Lỏng | 78,37 | -114 | ∞ | ∞ |
X, Y, Z tương ứng là chất nào sau đây:
Cho các thí nghiệm sau:
(1) Trộn dung dịch NaHCO3 dư với dung dịch Ba(OH)2.
(2) Sục khí CO2 dư vào dung dịch bari aluminat Ba(AlO2)2.
(3) Cho NaOH dư vào dung dịch CrCl3.
(4) Cho Ba(OH)2 dư vào dung dịch Al2(SO4)3.
Số thí nghiệm thu được kết tủa sau khi kết thúc là:
Hòa tan hoàn toàn m gam hỗn hợp X gồm Al và Al2O3 trong 500ml dung dịch chứa hỗn hợp NaOH 0,3M và Ba(OH)2 0,1M thu được dung dịch Y và 3,36 lít H2 (đktc). Cho dung dịch Y phản ứng với 500 ml dung dịch Z chứa HCl 0,64M và H2SO4 0,08M thu được 21,02 gam kết tủa. Nếu cho dung dịch Y phản ứng với V lít dung dịch Z thì thu được kết tủa lớn nhất có khối lượng a gam. Giá trị của a là:
Hỗn hợp gồm hexametylenđiamin, anilin, alanin và lysin (trong đó nguyên tố nitơ chiếm 20,22% khối lượng). Trung hòa m gam X bằng dung dịch H2SO4 vừa đủ, thu được 201,0 gam hỗn hợp muối. Giá trị của m là
Hỗn hợp gồm hexametylenđiamin, anilin, alanin và lysin (trong đó nguyên tố nitơ chiếm 20,22% khối lượng). Trung hòa m gam X bằng dung dịch H2SO4 vừa đủ, thu được 201,0 gam hỗn hợp muối. Giá trị của m là
Hỗn hợp X gồm 4 chất hữu cơ đều có cùng công thức phân tử C2H8O3N2. Cho một lượng X phản ứng vừa đủ với V ml dung dịch NaOH 0,5M và đun nóng, thu được dung dịch Y chỉ gồm các chất vô cơ và 6,72 lít (đktc) hỗn hợp Z gồm 3 amin. Cô cạn toàn bộ dung dịch Y thu được 29,28 gam hỗn hợp muối khan. Giá trị của V là
Chất hữu cơ Xcó công thức phân tử C4H6O4 không có khả năng tham gia phản ứng tráng bạc. Cho a mol X phản ứng với dung dịch KOH dư, thu được ancol Y và m gam một muối. Đốt cháy hoàn toàn một lượng ancol Y thu được 0,2 mol CO2 và 0,3 mol H2O. Giá trị của a và m lần lượt là
Tiến hành điện phân (điện cực trơ, màng ngăn) một dung dịch hỗn hợp RSO4 0,3M và KCl 0,2M với cường độ dòng điện I = 0,5A sau thời gian t giây thu được kim loại ở catot và 1,344 lít (đktc) hỗn hợp khí ở anot. Sau thời gian 3t giây thu được hỗn hợp khí có thể tích là 4,256 lít (đktc) hỗn hợp khí. Biết hiệu suất phản ứng 100%, R có hóa trị không đổi. Giá trị của t là
Thủy phân hoàn toàn một este E trong 500ml dung dịch NaOH 3M, cô cạn dung dịch sau phản ứng thu được 135,6 gam chất rắn và m gam hơi một ancol no, đơn chức, mạch hở X. Oxi hóa m gam ancol X thu được hỗn hợp Y gồm anđehit, axit, ancol dư và nước. Chia hỗn hợp thành 3 phần bằng nhau:
Phần 1: Cho vào dung dịch AgNO3/NH3 dư thu được 54 gam Ag.
Phần 2: Cho phản ứng vừa đủ với dung dịch nước brom thu được 3,36 lít khí Z (đktc) duy nhất.
Phần 3: Cho tác dụng với Na dư thu được 5,6 lít khí H2 (đktc)
Công thức cấu tạo của E là
E là hỗn hợp 3 peptit X, Y, Z. Thủy phân hoàn toàn 37 gam E cần dùng 450 ml dung dịch KOH 1M, sau phản ứng hoàn toàn cô cạn thu được hỗn hợp M gồm 3 muối kali của Gly, Ala và Lys với số mol tương ứng là x, y, z. Nếu đốt cháy hoàn toàn một lượng hỗn hợp peptit E thu được số mol CO2 và H2O bằng nhau. Nếu đốt cháy hỗn hợp gồm a mol muối kali của Gly và b mol muối kali của Ala (a.y = b.x) được 99 gam CO2 và 49,5 gam H2O. Phần trăm khối lượng muối của kali của Ala trong hỗn hợp muối M gần nhất với giá trị nào sau đây?
Hỗn hợp P gồm 2 axit đa chức X, Y có số mol bằng nhau và axit đơn chức Z (X, Y, Z đều mạch hở, không phân nhánh và có số nguyên tử C không lớn hơn 4; MX < MY). Trung hòa m gam hỗn hợp P cần vừa đủ 510 ml dung dịch NaOH 1M. Đốt cháy hoàn toàn m gam P thu được CO2 và 7,02 gam H2O. Còn nếu cho m gam P tác dụng với AgNO3/NH3 dư thì thu được 52,38 gam kết tủa. Nhận định nào sau đây đúng?
Đề thi tương tự
1 mã đề 40 câu hỏi 1 giờ
136,615 xem10,503 thi
