Đề thi thử THPT QG môn Hóa học năm 2018
Đề thi nằm trong bộ sưu tập: 📘 Tuyển Tập Bộ Đề Thi Ôn Luyện THPT Quốc Gia Môn Hóa Học Các Trường (2018-2025) - Có Đáp Án Chi Tiết 🧪📘 Tuyển Tập Đề Thi Tham Khảo Các Môn THPT Quốc Gia 2025 🎯
Số câu hỏi: 40 câuSố mã đề: 1 đềThời gian: 1 giờ
103,093 lượt xem 7,924 lượt làm bài
Xem trước nội dung:
Dung dịch có pH > 7 tác dụng được với dung dịch K2SO4 tạo kết tủa là
Cho vài giọt dung dịch H2S vào dung dịch FeCl3 hiện tượng xảy ra là
Cấu hình electron của ion Cr3+ là
Đồng phân là những chất
Chất nào sau đây có thể oxi hóa Zn thành Zn2+?
Thành phần chính của khí than ướt là
Cho các polime sau đây: (1) tơ tằm; (2) sợi bông; (3) sợi đay; (4) tơ enang; (5) tơ visco; (6) nilon-6,6; (7) tơ axetat. Loại tơ có nguồn gốc xenlulozơ là
Cho một số nhận định về nguyên nhân gây ô nhiễm không khí như sau:
(a) do khí thải từ quá trình quang hợp cây xanh;
(b) do hoạt động của núi lửa;
(c) do khí thải công nghiệp.
Các nhận định đúng là
Nhiệt phân hoàn toàn 100 gam mẫu đá vôi thu được 20,37 lít CO2 ở đktc. Tìm hàm lượng phần trăm của CaCO3.
Chất hữu cơ X mạch thẳng có CTPT C4H6O2.
Biết X (+ dung dịch NaOH) → A (+ NaOH/CaO, to) → Etilen
Công thức cấu tạo của X là
Cho các chất sau: đietylete, vinyl axetat, saccarozơ, tinh bột, vinyl clorua, nilon-6,6. Số chất bị thủy phân trong môi trường kiềm nóng là
Triolein không tác dụng với chất (hoặc dung dịch) nào sau đây?
Cho 142 gam P2O5 vào 500 gam dung dịch H3PO4 23,72% được dung dịch A. Tìm nồng độ % của dung dịch A.
Phenol phản ứng được với dung dịch nào sau đây?
Phát biểu nào sau đây sai?
Thực hiện lên men ancol từ glucozơ (hiệu suất lên men 80%) được etanol và khí CO2. Dẫn khí thu được vào dung dịch nước vôi trong dư thu được 40 gam kết tủa. Lượng glucozơ ban đầu là
Tiến hành phản ứng theo sơ đồ hình vẽ
Oxit X là
Một mẫu nước có chứa các ion: Ca2+, Mg2+, HCO3–, Cl –. Mẫu nước trên thuộc loại
Dãy các hợp chất tác dụng được với dung dịch HCl vào dung dịch NaOH là
Có 4 dung dịch riêng biệt: HCl, FeCl2, AgNO3, CuSO4. Nhúng vào dung dịch một thanh sắt nguyên chất. Số trường hợp xuất hiện ăn mòn hóa học là
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch AgNO3 vào dung dịch HCl dư.
(b) Cho Al2O3 vào dung dịch H2SO4 loãng dư.
(c) Cho Cu vào dung dịch HNO3 loãng dư.
(d) Cho dung dịch NaOH vào dung dịch Ca(HCO3)2.
Sau khi kết thúc các phản ứng, số trường hợp thu được chất rắn là
Đun nóng m gam hỗn hợp X gồm các chất có cùng một loại nhóm chức với 720 ml dd NaOH 1,15M, thu được dd Y chứa muối của một axit cacboxylic đơn chức và 18,48 gam hơi Z gồm các ancol. Cho toàn bộ Z tác dụng với Na dư, thu được 6,048 lít khí H2 (đktc). Cô cạn dd Y, nung nóng chất rắn thu được với CaO cho đến khi phản ứng xảy ra hoàn toàn, thu được 8,64 gam một chất khí. Giá trị của m gần nhất với
Hai este A, B là dẫn xuất của benzen có công thức phân tử là C9H8O2, A và B đều cộng hợp với brom theo tỉ lệ mol là 1:1. A tác dụng với dd NaOH cho một muối và một andehit. B tác dụng với dd NaOH dư cho 2 muối và nước, các muối đều có phân tử khối lớn hơn phân tử khối của CH3COONa. Công thức cấu tạo thu gọn của A và B lần lượt là
Nung 896 ml C2H2 và 1,12 lít H2 (đktc) với Ni (với hiệu suất H = 100%) được hỗn hợp X gồm 3 chất. dẫn X qua dung dịch AgNO3 trong NH3 dư, được 2,4 gam kết tủa. Số mol của phân tử khối lớn nhất trong X là
Hỗn hợp A gồm axit oxalic, axetilen, propanđial và vinylfomat (trong đó số mol của axit oxalic và axetilen bằng nhau). Đốt cháy hoàn toàn m gam hỗn hợp A cần dùng vừa đủ 1,35 mol O2, thu được H2O và 66 gam CO2. Nếu cho m gam hỗn hợp X tác dụng với dd NaHCO3 dư thì thu được tối đa bao nhiêu lít CO2 (đktc).
Cho 20 gam hỗn hợp gồm 3 amin no, đơn chức, là đồng đẳng liên tiếp của nhau (được trộn theo tỉ lẹ mol 1 : 10 : 5 và thứ tự phân tử khối tăng dần) tác dụng vừa đủ với dd HCl, thu được 31,68 gam hỗn hợp muối. Công thức phân tử của ba amin là
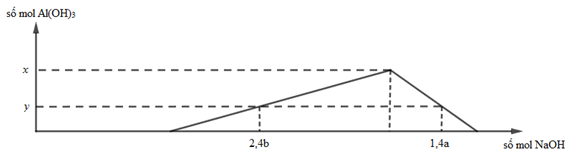
Cho từ từ đến dư dd NaOH 0,1M vào 300 ml dd hỗn hợp gồm H2SO4 a mol/lít và Al2(SO4)3 b mol/lít. Đồ thị nào dưới đây mô tả sự phụ thuộc của số mol kết tủa Al(OH)3 vào số mol NaOH đã dùng.
Tỉ số gần giá trị nào nhất sau đây?
Cho sơ đồ:
Ca3(PO4)2 + (SiO2, 1200oC) → A (+ Ca, to) → B (+ HCl) → C (+O2,to) → D
Vậy A, B, C, D lần lượt là
Hỗn hợp E gồm este X đơn chức và axit cacboxylic Y hai chức (đều mạch hở, không no, có một liên kết đôi C=C trong phân tử). Đốt cháy hoàn toàn một lượng E thu được 0,86 mol khí CO2 và 0,64 mol hơi nước. Mặt khác, thủy phân 93,2 gam E bằng 400 gam dung dịch NaOH 12% rồi cô cạn dung dịch thu được phần hơi Z có chứa chất hữu cơ T. Dẫn toàn bộ vào bình đựng Na, sau phản ứng khối lượng bình tăng 377,7 gam đồng thời thoát ra 12,32 lít khí H2 (đktc). Biết tỉ khối của T so với H2 là 16. Phần trăm khối lượng của Y trong hỗn hợp E có giá trị gần nhất với giá trị nào sau đây?
Đốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với hỗn hợp khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho dung dịch Z tác dụng hoàn toàn với lượng dư AgNO3, thu được 56,69 gam kết tủa. Phần trăm thể tích của clo trong hỗn hợp X gần với giá trị nào nhất sau đây ?
Khi cho 121,26 gam hợp kim gồm có Fe, Al và Cr tác dụng với một lượng dư dd kiềm, thu được 6,048 lít (đktc). Lấy bã rắn không tan cho tác dụng với một lượng dư axit clohidric (khí không có không khí) thu được 47,04 lít (đktc) khí. Thành phần phần trăm theo khối lượng Cr trong hợp kim bằng
Cho 86,3 gam hỗn hợp X gồm Na, K, Ba và Al2O3 (trong đó oxi chiếm 19,47% về khối lượng) tan hết vào nước, thu được dung dịch Y và 13,44 lít khí H2(đktc). Cho 3,2 lít dung dịch HCl0,75M vào dung dịch Y. Sau khi các phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là:
Phát biểu nào sau đây đúng?
Hỗn hợp E gồm chất X (C3H10N2O4) và chất Y (C3H12N2O3). X là muối của axit hữu cơ đa chức, Y là muối của một axit vô cơ. Cho m gam E tác dụng với dung dịch NaOH dư, đun nóng, thu được 0,072 mol hai khí (có tỉ lệ mol 1: 5) và dung dịch chứa a gam muối. Giá trị của m là
Hỗn hợp X gồm KCl và KClO3. Người ta cho thêm 10 gam MnO2 vào 39,4 gam hỗn hợp X thu được hỗn hợp Y. Nung y ở nhiệt độ cao được chất rắn Z và khí P. Cho Z vào dung dịch AgNO3 lấy dư thu được 67,4 gam chất rắn. Lấy 1/3 khí P sục vào dung dịch chứa 0,5 mol FeSO4 và 0,3 mol H2SO4 thu được dung dịch Q. Cho dung dịch Ba(OH)2 lấy dư vào dung dịch Q thu được kết tủa. Biết các phản ứng hoàn toàn. Giá trị của X là
Điện phân dd Cu(NO3)2 điện cực trơ, với cường độ dòng điện 3A, thu được dd X chứa hai chất tan có cùng nồng độ mol. Nhúng một thanh Fe vào dd X đến khi phản ứng xảy ra hoàn toàn, thu được khí NO là sản phẩm khử duy nhất, rút thành Fe ra cân lại thấy khối lượng thanh Fe giảm 1,56 gam so với ban đầu. Thời gian điện phân là
Cho sơ đồ chuyển hóa sau:
C2H4 (+ Br2) → A1 (+ NaOH) → A2 (+ CuO) → A3 (+ Cu(OH)2, NaOH) → A4 (+ H2SO4) → A5
Chọn câu trả lời sai
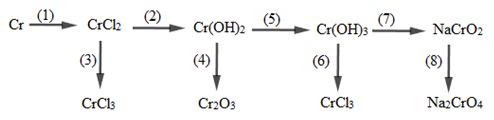
Cho sơ đồ chuyển hóa sau
Số phản ứng oxi hóa - khử xảy ra trong sơ đồ trên là
Thủy phân hoàn toàn 0,09 mol hỗn hợp X gồm tripeptit, tetapeptit, pentapetit với dung dịch NaOH vừa đủ thu được 16,49 gam muối của Glyxin, 17,76 gam muối của Alanin và 6,95 gam muối của Valin. Nếu đốt cháy hoàn toàn m gam hỗn hợp X thì thu được CO2, H2O và N2 trong đó tổng khối lượng của CO2 và H2O là 46,5 gam. Giá trị gần đúng của m là
Thủy phân hoàn toàn 1 mol pentapeptit X, thu được 2 mol glyxin (Gly), 1 mol alanin (Ala), 1 mol Valin (Val), và 1 mol phenylalanin (Phe). Thủy phân không hoàn toàn X thu được đipeptit Val-Phe và tripeptit Gly-Ala-Val nhưng không thu được đipeptit Gly-Gly. Chất X có công thức là

.PNG)