
[2022] Trường THPT Lê Quý Đôn - Đề thi thử THPT QG năm 2022 môn Hóa học
Đề thi nằm trong bộ sưu tập: 📘 Tuyển Tập Bộ Đề Thi Ôn Luyện THPT Quốc Gia Môn Hóa Học Các Trường (2018-2025) - Có Đáp Án Chi Tiết 🧪📘 Tuyển Tập Đề Thi Tham Khảo Các Môn THPT Quốc Gia 2025 🎯
Số câu hỏi: 40 câuSố mã đề: 1 đềThời gian: 1 giờ
203,997 lượt xem 15,686 lượt làm bài
Xem trước nội dung:
Khi thuỷ phân đến cùng protein thu được
Polime được điều chế bằng phản ứng trùng hợp là
Khi thuỷ phân bất kỳ chất béo nào cũng thu được
Nếu bỏ qua sự phân li của nước, số loại ion trong dung dịch axit photphoric là bao nhiêu?
Nếu thuỷ phân không hoàn toàn pentapeptit Gly-Ala-Gly-Val-Ala thì thu được tối đa bao nhiêu đipeptit mạch hở chứa Gly?
Tơ lapsan thuộc loại
Để đo nồng độ cồn (C2H5OH) trong máu, cảnh sát giao thông sử dụng các dụng cụ phân tích có chứa
Phương trình hoá học nào sau đây thể hiện cách điều chế Cu theo phương pháp thuỷ luyện? (Biết phản ứng đã xảy ra trong điều kiện thích hợp)
Trong dung dịch, ion CO32- có thể cùng tồn tại với dãy các ion nào sau đây?
Khi nói về CO2, khẳng định nào sau đây không đúng?
Thuỷ phân este X có công thức phân tử là C4H6O2 trong môi trường axit, thu được một hỗn hợp các chất đều tham gia phản ứng tráng gương. Vậy công thức cấu tạo của X là?
Phát biểu nào sau đây đúng?
Trộn dung dịch chứa x mol AlCl3 với dung dịch chứa y mol NaOH. Để thu được kết tủa thì cần có tỉ lệ
Tiến hành sục khí Cl2 vào dung dịch CrCl3 trong môi trường NaOH. Sản phẩm thu được là
Cho 9,125 gam amin đơn chức X phản ứng hoàn toàn với HCl (dư), thu được 13,6875 gam muối. Số đồng phân cấu tạo của X là
Hỗn hợp X gồm ancol metylic, etylen glicol. Cho m gam X phản ứng hoàn toàn với Na dư, thu được 2,24 lít khí H2 (đktc). Đốt cháy hoàn toàn m gam X, thu được a gam CO2. Giá trị của a là
Dung dịch X chứa hỗn hợp các chất KOH 0,05M, NaOH 0,05M và Ca(OH)2 0,15M. Sục 7,84 lít khí CO2 (đktc) vào 1 lít dung dịch X thì lượng kết tủa thu được là?
Hiđrocacbon thơm E có công thức cấu tạo như sau
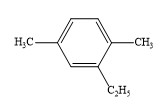
Tên gọi của E theo danh pháp thay thế là
X là một este hữu cơ đơn chức, mạch hở. Cho một lượng X tác dụng hoàn toàn với dung dịch NaOH vừa đủ, thu được muối có khối lượng bằng khối lượng este ban đầu. X là?
Cho 11,5 gam hỗn hợp các kim loại Al, Cr, Fe tác dụng với lượng dư dung dịch H2SO4 loãng nóng (trong điều kiện không có không khí), thu được dung dịch X và 5,6 lít khí H2 (ở đktc). Cô cạn dung dịch X (trong điều kiện không có không khí) được m gam muối khan. Giá trị của m là
Cho các sơ đồ phản ứng sau:
\begin{align} & {{C}_{8}}{{H}_{14}}{{O}_{4}}+NaOH\xrightarrow{{}}{{X}_{1}}+{{X}_{2}}+{{H}_{2}}O \\ & {{X}_{1}}+{{H}_{2}}S{{O}_{4}}\xrightarrow{{}}{{X}_{3}}+N{{a}_{2}}S{{O}_{4}} \\ & {{X}_{3}}+{{X}_{4}}\xrightarrow{{}}Nilon-6,6+{{H}_{2}}O \\\end{align}
Phát biểu nào sau đây đúng?
Hoà tan hoàn toàn 15,6 gam hỗn hợp Al và Al2O3 vào dung dịch Ba(OH)2 dư, thu được dung dịch X và thoát ra V lít H2 (đktc). Cho từ từ đến dư dung dịch H2SO4 loãng vào X thì thấy lượng H2SO4 phản ứng tối đa là 0,9 mol, đồng thời thu được 69,9 gam kết tủa. Giá trị của V là
Điện phân dung dịch AgNO3 (điện cực trơ) trong thời gian 20 phút, thu được 0,54 gam Ag ở catot. Sau đó để làm kết tủa hết ion Ag+ còn lại trong dung dịch sau điện phân cần dùng 30 ml dung dịch NaCl 0,5M. Cường độ dòng điện và khối lượng AgNO3 ban đầu tương ứng là?
Cho m gam tinh bột lên men thành C2H5OH với hiệu suất 81%, hấp thụ hết lượng CO2 sinh ra vào dung dịch Ca(OH)2 được 55 gam kết tủa và dung dịch X. Đun nóng dung dịch X lại có 10 gam kết tủa nữa. Giá trị m là
Valin là một loại amino axit thiết yếu, cần được cung cấp từ nguồn thực phẩm bên ngoài, cơ thể không tự tổng hợp được. Khi cho 1,755 gam valin hoà tan trong nước thu được dung dịch X. Dung dịch X phản ứng vừa đủ với 15 ml dung dịch NaOH có nồng độ C (mol/l). Giá trị của C là
Đun nóng m gam một hợp chất hữu cơ X (chứa C, H, O), mạch không phân nhánh với dung dịch chứa 11,2 gam KOH đến khi phản ứng xảy ra hoàn toàn, thu được dung dịch A, để trung hoà dung dịch KOH dư trong A cần dùng 80 ml dung dịch HCl 0,5M. Làm bay hơi hỗn hợp sau khi trung hoà một cách cẩn thận, người ta thu được 7,36 gam hỗn hợp hai ancol đơn chức Y và 18,34 gam hỗn hợp hai muối Z. Giá trị của m là
Dẫn V lít (đktc) hỗn hợp X gồm axetilen và hiđro có khối lượng là m gam đi qua ống sứ đựng bột niken nung nóng, thu được khí Y. Dẫn Y vào lượng dư AgNO3 trong dung dịch NH3 thu được 12 gam kết tủa. Khi đi ra khỏi dung dịch phản ứng vừa đủ với 16 gam brom và còn lại khí Z. Đốt cháy hoàn toàn khí Z thu được 2,24 lít khí CO2 (đktc) và 4,5 gam H2O. Giá trị của V là
Hỗn hợp X gồm Ala-Ala, Gly-Ala, Ala-Gly, Ala-Ala-Val-Ala và Ala-Val-Val-Ala. Cho m gam hỗn hợp X tác dụng với lượng vừa đủ NaOH, đun nóng thu được m+29,7 gam hỗn hợp muối của các amino axit. Mặt khác nếu đốt cháy hoàn toàn m gam hỗn hợp X thu được 63,616 lít CO2 (đktc) và 49,32 gam H2O. Giá trị gần đúng của m là
Hoà tan hoàn toàn hai chất rắn X, Y vào nước thu được dung dịch Z. Tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho dung dịch KOH dư vào V lít dung dịch Z, đun nóng thu được n1 mol khí.
Thí nghiệm 2: Cho dung dịch H2SO4 dư vào V lít dung dịch Z, thu được n2 mol khí không màu hoá nâu ngoài không khí, là sản phẩm khử duy nhất.
Thí nghiệm 3: Cho dung dịch Ba(OH)2 dư vào V lít dung dịch Z, thu được n1 mol kết tủa.
Biết các phản ứng xảy ra hoàn toàn và n1 = 6n2. Hai chất rắn X, Y lần lượt là?
Cho các phát biểu sau:
(a) Đốt cháy hoàn toàn este no, đơn chức, mạch hở luôn thu được số mol CO2 bằng số mol H2O.
(b) Các loại bật lửa ga thông dụng trên thị trường chứa nguyên liệu chủ yếu là khí metan hoá lỏng
(c) Bậc của amin là bậc của nguyên tử cacbon liên kết với nhóm amin.
(d) Để hạn chế vị tanh của cá, khi nấu canh cá người ta nấu với các loại có vị chua như me, sấu, khế…
(e) Có thể phân biệt len (lông cừu) và “len” (tơ nitron) bằng cách đốt.
Số phát biểu đúng là?
Các hiđroxit: NaOH, Al(OH)3, Fe(OH)3, Ba(OH)2 được kí hiệu ngẫu nhiên là X, Y, Z, T. Kết quả thí nghiệm của X, Y, Z, T được ghi ở bảng sau:
X | Y | Z | T | |
Tính tan | Tan | Không tan | Không tan | Tan |
Phản ứng với NaOH | Không xảy ra phản ứng | Không xảy ra phản ứng | Có xảy ra phản ứng | Không xảy ra phản ứng |
Phản ứng với Na2SO4 | Không xảy ra phản ứng | Không xảy ra phản ứng | Không xảy ra phản ứng | Phản ứng tạo kết tủa trắng |
Các chất X, Y, Z, T lần lượt là
Một học sinh lắp đặt dụng cụ thí nghiệm như hình dưới đây từ các chất X, Y để điều chế khí Z. Phản ứng hoá học thoả mãn thí nghiệm trên là?
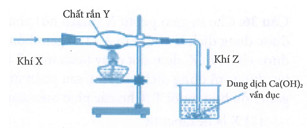
Tiến hành các thí nghiệm sau
(a) Cho dung dịch NH3 dư vào dung dịch BaCl2.
(b) Cho dung dịch FeCl3 vào dung dịch H2S.
(c) Cho dung dịch AgNO3 vào dung dịch H3PO4.
(d) Cho dung dịch AgNO3 dư vào dung dịch Fe(NO3)2.
(e) Cho dung dịch AlCl3 vào dung dịch H2S.
Sau khi thí nghiệm kết thúc, số trường hợp thu được kết tủa là
Dung dịch X chứa hỗn hợp muối KCl a mol và CuSO4 b mol (trong đó a < 2b). Tiến hành điện phân dung dịch với điện cực trơ với thời gian t giây. Giả thiết thể tích dung dịch không đổi trong quá trình điện phân. Giá trị pH của dung dịch biến đổi theo đồ thị nào sau đây?
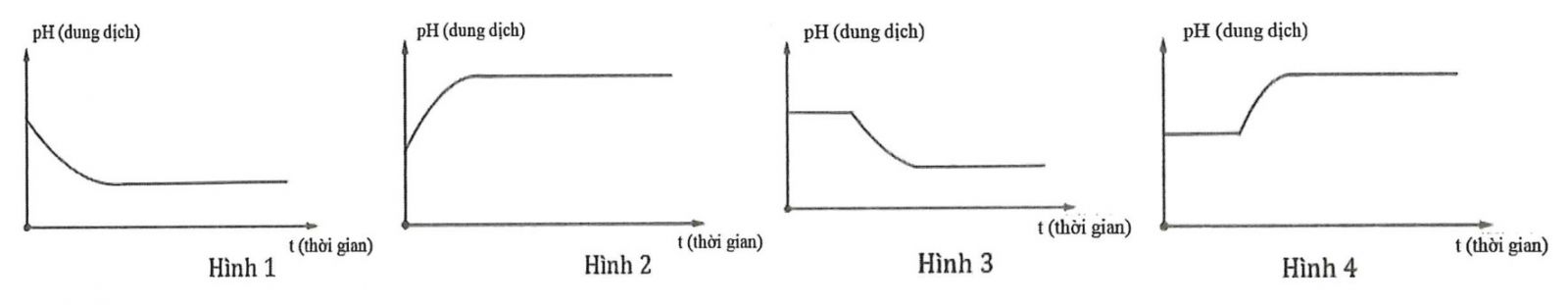
Tiến hành các thí nghiệm sau:
(1) Cho Mg vào dung dịch Fe2(SO4)3 dư.
(2) Cho bột Zn vào lượng dư dung dịch HCl.
(3) Dẫn khí H2 dư qua ống sứ chứa bột CuO nung nóng.
(4) Cho Ba vào lượng dư dung dịch CuSO4.
(5) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là
Cho m gam peptit X (mạch hở) phản ứng vừa đủ dung dịch NaOH đun nóng, thu được dung dịch Y chứa (m + 11,1) gam hỗn hợp muối natri của Gly, Ala và Val. Cô cạn Y được chất rắn Z, đem đốt cháy hoàn toàn Z thu được 15,9 gam Na2CO3. Nếu cho m gam X tác dụng với dung dịch HCl dư, sau phản ứng dung dịch thu được đem cô cạn được 36,25 gam hỗn hợp muối T. Cho các phát biểu sau:
(1) X là hexapeptit (3) Phân tử khối của X là 416 (5) % khối lượng muối clorua của Gly trong T là 46,4% | (2) Giá trị của m = 20,8 gam (4) Trong X chỉ có 1 gốc Ala |
Số phát biểu đúng là
Cho m1 gam hỗn hợp X chứa Al, Fe(NO3)2 và 0,1 mol Fe3O4 tan hết trong dung dịch chứa 1,025 mol H2SO4. Sau phản ứng thu được 5,04 lít (đktc) hỗn hợp khí Y gồm hai khí trong đó có một khí hoá nâu ngoài không khí và dung dịch Z chỉ chứa các muối sunfat trung hoà. Biết tỷ khối của Y so với H2 là 31/3. Cho một lượng vừa đủ BaCl2 vào Z sau khi các phản ứng xảy ra xong cho tiếp AgNO3 dư vào thì thu được m2 gam kết tủa. Biết các phản ứng hoàn toàn. Giá trị của tổng m1 + m2 là:
X, Y là hai axit cacboxylic đều đơn chức, mạch hở (trong mỗi phân tử X, Y chứa không quá 2 liên kết và 50 < MX < MY); Z là este được tạo bởi X, Y và etylen glicol. Đốt cháy 13,12 gam hỗn hợp E chứa X, Y, Z cần dùng 0,5 mol O2. Mặt khác, cho 0,36 mol E làm mất màu vừa đủ dung dịch chứa 0,1 mol Br2. Nếu đun nóng 13,12 gam E với 200 ml dung dịch KOH 1M (vừa đủ), cô cạn dung dịch sau phản ứng thu được hỗn hợp F gồm a gam muối P và b gam muối Q (MP < MQ). Tỉ lệ a: b gần nhất với giá trị nào sau đây?
Hoà tan hoàn toàn 11,2648 gam hỗn hợp X gồm Fe, Fe(NO3)2 và Al vào dung dịch HCl vừa đủ. Sau phản ứng hoàn toàn, thu được dung dịch Y có chứa 24,2348 gam muối và thoát ra 0,672 lít hỗn hợp khí Z gồm 2 khí không màu, đều nhẹ hơn không khí. Cho dung dịch Y tác dụng với dung dịch AgNO3 dư thì thu được 72,2092 gam kết tủa. % khối lượng muối FeCl3 trong hỗn hợp muối là.
Hoà tan hoàn toàn m gam hỗn hợp X gồm Mg, Fe, FeCO3, Cu(NO3)2 vào dung dịch chứa H2SO4 và 0,045 mol NaNO3, thu được dung dịch Y chỉ chứa 62,605 gam muối trung hoà và 3,808 lít (đktc) hỗn hợp Z (trong đó có 0,02 mol H2, NO, CO2). Tỉ khối của Z so với O2 bằng 19/17. Thêm dung dịch NaOH 1M vào Y đến khi thu được lượng kết tủa lớn nhất là 31,72 gam thì vừa hết 865 ml. Mặt khác, cho Y tác dụng vừa đủ với BaCl2, sau đó cho tiếp tục lượng dư AgNO3 vào thu được 256,04 gam kết tủa. Thành phần phần trăm về khối lượng của kim loại Fe trong hỗn hợp X gần nhất với?
Đề thi tương tự
1 mã đề 50 câu hỏi 1 giờ
215,990 xem16,603 thi
1 mã đề 40 câu hỏi 1 giờ
193,536 xem14,875 thi
1 mã đề 40 câu hỏi 1 giờ
209,419 xem16,103 thi
1 mã đề 40 câu hỏi 1 giờ
206,279 xem15,858 thi
1 mã đề 40 câu hỏi 50 phút
201,102 xem15,459 thi
1 mã đề 40 câu hỏi 1 giờ
220,539 xem16,953 thi
1 mã đề 50 câu hỏi 1 giờ
204,771 xem15,743 thi
1 mã đề 40 câu hỏi 1 giờ
205,327 xem15,781 thi
1 mã đề 40 câu hỏi 1 giờ
201,933 xem15,527 thi
