Đề thi thử THPT QG môn Hóa học năm 2018
Thời gian làm bài: 1 giờ
Đề thi nằm trong bộ sưu tập: 📘 Tuyển Tập Bộ Đề Thi Ôn Luyện THPT Quốc Gia Môn Hóa Học Các Trường (2018-2025) - Có Đáp Án Chi Tiết 🧪
Hãy bắt đầu chinh phục nào!
Xem trước nội dung:
Công thức nào sau đây là công thức của chất béo?
Trộn bột kim loại X với bột sắt oxit (gọi là hỗn hợp tecmit) để thực hiện phản ứng nhiệt nhôm dùng để hàn đường ray tàu hỏa. Kim loại X là:
Ô nhiễm không khí có thể tạo ra mưa axit, gây ra tác hại rất lớn với môi trường. Hai khí nào sau đây là nguyên nhân gây ra mưa axit?
Kim loại mà khi tác dụng với HCl hoặc Cl2 không cho ra cùng một muối là:
Chất không có khả năng làm xanh quỳ tím là:
Cho Fe tác dụng với HNO3 đặc nóng thu được khí X có màu nâu đỏ. Khí X là:
Kim loại có nhiệt độ nóng chảy cao nhất có ký hiệu hóa học là:
Chất không bị nhiệt phân hủy là
Hợp chất H2NCH2COOH có tên gọi là
Trong công nghiệp, kim loại nào sau đây chỉ được điều chế bằng phương pháp điện phân nóng chảy?
Cho các hợp kim sau: Cu–Fe (1); Zn–Fe (II); Fe–C (III); Sn–Fe (IV). Khi tiếp xúc với dung dịch chất điện li thì các hợp kim mà trong đó Fe đều bị ăn mòn trước là
Cho các chất: anlyl axetat, phenyl axetat, etyl fomat, tripanmitin. Số chất trong các chất khí trên khi thủy phân trong dung dịch NaOH dư, đun nóng sinh ra ancol là
Một số hợp chất hữu cơ mạch hở, thành phần chứa C, H, O và có khối lượng phân tử 60 đvC. Trong các chất trên, số chất tác dụng được với Na là:
Cho từ từ 200 ml dung dịch hỗn hợp HCl 1M và H2SO4 0,5M vào 300 ml dung dịch Na2CO3 1M thu được V lít khí (ở đktc). Giá trị của V là:
Cho hỗn hợp X gồm Fe2O3, ZnO, Cu tác dụng với dung dịch HCl (dư) thu được dung dịch Y và phần không tan Z. Cho Y tác dụng với dung dịch NaOH (loãng dư) thu được kết tủa gồm:
Hòa tan hoàn toàn 3,2 gam một oxit kim loại cần vừa đủ 40 ml dung dịch HCl 2M. Công thức của oxit đó là:
Dãy các chất đều có khả năng tham gia phản ứng thủy phân trong dung dịch H2SO4 loãng, nóng là:
Dẫn luồng khí CO dư qua hỗn hợp CuO, Al2O3, CaO, MgO có số mol bằng nhau (nung nóng ở nhiệt độ cao) thu được chất rắn A. Hòa tan A vào nước dư còn lại chất rắn X. X gồm:
Cho 23,00 gam C2H5OH tác dụng với 24,00 gam CH3COOH (to, xúc tác H2SO4 đặc) với hiệu suất phản ứng 60%. Khối lượng este thu được là
Este C4H8O2 tác dụng với dung dịch NaOH tạo ra ancol etylic. Công thức cấu tạo của este đó là:
Có các phát biểu sau:
(1) Kim loại Cu khử được ion Fe2+ trong dung dịch.
(2) Thạch cao nung được dùng để đúc tượng, bó bột khi gãy xương, làm phấn viết bảng,...
(3) SO3 khi tác dụng với nước tạo thành 2 axit.
(4) Al(OH)3 vừa tác dụng được với dung dịch NaOH vừa tác dụng được với dung dịch HCl.
(5) CuSO4 khan được dùng để phát hiện dấu vết nước trong chất lỏng.
Số phát biểu đúng là
Cho dãy các chất: metan, etin, eten, etanol, etanoic, propenoic, benzen, alanin, phenol, triolein. Số chất trong dãy làm mất màu dung dịch brom là:
Tiến hành các thí nghiệm:
(1) Cho AgNO3 vào dung dịch Fe(NO3)2.
(2) Dẫn NH3 qua ống đựng CuO nung nóng.
(3) Cho Al vào dung dịch Fe2(SO4)3 dư.
(4) Cho K vào dung dịch Cu(NO3)2.
Sau khi kết thúc phản ứng, số thí nghiệm có tạo thành kim loại là
Cho các phát biểu:
(a) Chất béo là trieste của glixerol với axit béo.
(b) Glucozơ thuộc loại monosaccarit.
(c) Tất cả các peptit đều có phản ứng với Cu(OH)2 tạo hợp chất màu tím.
(d) Dung dịch saccarozơ không tham gia phản ứng tráng bạc.
Số phát biểu đúng là
Khi cho các chất Al, FeS, dung dịch HCl, dung dịch NaOH và dung dịch (NH4)2CO3 phản ứng với nhau từng đôi một thì số chất khí có thể thu được là:
Cho các chất : Al,AlCl3, Zn(OH)2, NH4HCO3, KHSO4, NaHS, Fe(NO3)2. Số chất vừa phản ứng với dung dịch NaOH vừa phản ứng với dung dịch HCl là:
Cho các chất: AgNO3, Cu(NO3)2, MgCO3, CaCO3, Ba(HCO3)2, NH4HCO3, NH4NO3 và Fe(NO3)2. Nếu nung các chất trên đến khối lượng không đổi trong các bình kín không có không khí, rồi cho nước vào các bình, số bình có thể tạo lại chất ban đầu sau thí nghiệm là:
Hợp chất mạch hở X, có công thức phân tử C4H8O3. Khi cho X tác dụng với dung dịch NaOH đun nóng, thu được muối Y và ancol Z. Ancol Z hòa tan được Cu(OH)2. Số đồng phân cấu tạo thỏa mãn điều kiện trên của X là:
Cho các dung dịch: CH3COOH, C2H4(OH)2, C3H5(OH)3, glucozơ, saccarozơ, C2H5OH, anbumin (có trong lòng trắng trứng). Số dung dịch phản ứng được với Cu(OH)2 là:
Một dung dịch X chứa 0,01 mol Ba2+, 0,01 mol NO3–, a mol OH–, b mol Na+. Để trung hòa lượng dung dịch X này cần dùng 400 ml dung dịch HCl có pH = 1. Khối lượng chất rắn thu được sau khi cô cạn dung dịch X nói trên là
Đốt cháy hoàn toàn hỗn hợp X gồm các chất có công thức phân tử CH2O, CH2O2, C2H2O2 đều có cấu tạo mạch hở và có số mol bằng nhau thu được CO2, H2O. Hấp thụ hết sản phẩm cháy bằng nước vôi trong dư, sau phản ứng thấy khối lượng dung dịch giảm 17,0 gam so với khối lượng nước vôi trong ban đầu. Cho lượng hỗn hợp X như trên tác dụng với lượng dư dung dịch AgNO3 trong NH3 thì thu được tối đa m gam Ag. Giá trị của m là:
Hỗn hợp M gồm một este no đơn chức mạch hở và hai amin no, đơn chức mạch hở X và Y là đồng đẳng kế tiếp nhau (MX < MY). Đốt cháy hoàn toàn một lượng M cần dùng vừa đủ 0,225 mol O2, thu được H2O, N2 và 0,12 mol CO2. Công thức phân tử của Y là:
Cho Zn tới dư vào dung dịch gồm HCl ; 0,05 mol NaNO3 và 0,10 mol KNO3. Sau khi kết thúc các phản ứng thu được dung dịch X chứa m gam muối; 0,125 mol hỗn hợp khí Y gồm hai khí không màu, trong đó có một khí hóa nâu trong không khí. Tỉ khối của Y so với H2 là 12,2. Giá trị gần nhất của m là:
Hỗn hợp M gồm một peptit X và một peptit Y (mỗi peptit được cấu tạo từ một loại amino axit, tổng số nhóm -CO-NH- trong hai phân tử X và Y là 5) với tỉ lệ số mol nX : nY = 1:3. Khi thủy phân hoàn toàn m gam M thu được 81 gam glyxin và 42,72 gam alanin. m có giá trị là;
Hòa tan hoàn toàn 42,90 gam Zn trong lượng vừa đủ V mol dung dịch HNO3 10% (d = 1,26 g/ml), sau phản ứng thu được dung dịch A chứa 129,54 gam hai muối tan và 4,032 lít (ở đktc) hỗn hợp 2 khí NO và N2O. Giá trị của V là:
Hỗn hợp X gồm hai chất hữu cơ no, mạch hở (đều chứa C, H, O), trong phân tử mỗi chất có hai nhóm chức trong số các nhóm –OH, –CHO, –COOH. Cho m gam X phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 4,05 gam Ag và 1,86 gam muối amoni hữu cơ. Cho toàn bộ lượng muối amoni hữu cơ vào dung dịch NaOH (dư, đun nóng), thu được 0,02 mol NH3. Giá trị của m là
Cho hai bình điện phân, bình (I) đựng 20 ml dung dịch NaOH 1,73 M; bình (2) đựng dung dịch gồm 0,225 mol Cu(NO3)2 và 0,2 mol HCl. Mắc nối tiếp bình (1) và bình (2). Điện phân các dung dịch bằng dòng điện một chiều với cường độ dòng điện không đổi một thời gian. Khi dừng điện phân, tháo ngay catot ở các bình. Sau phản ứng thấy nồng độ NaOH ở bình (1) là 2M. Cho tiếp 14 gam bột Fe vào bình (2) đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn không tan. Biết NO là sản phẩm khử duy nhất của N+5 .Giá trị m là:
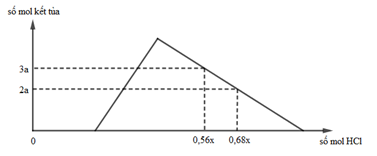
Hỗn hợp X gồm Al, Ca, Al4C3 và CaC2. Cho 40,3 gam X vào nước dư, chỉ thu được dung dịch Y và hỗn hợp khí Z (C2H2, CH4, H2). Đốt cháy hết Z thu được 20,16 lít khí CO2 (đktc) và 20,7 gam H2O. Nhỏ từ từ V lít dung dịch HCl xM vào Y, được biểu diễn theo hình vẽ:
Giá trị của x gần nhất với
Cho 11,2 lít hỗn hợp X gồm axetilen và anđehit axetic (ở đktc) qua dung dịch AgNO3/NH3 dư. Sau khi phản ứng hoàn toàn thu được 112,8 gam kết tủa. Dẫn lượng hỗn hợp X như trên qua dung dịch nước brom dư, khối lượng brom tham gia phản ứng là (giả sử lượng axetilen phản ứng với nước là không đáng kể).
Cho m kg một loại quặng apatit (chứa 93% khối lượng Ca3(PO4)2, còn lại là tạp chất trơ không chứa photpho) tác dụng vừa đủ với H2SO4 đặc để sản xuất supephotphat đơn. Độ dinh dưỡng của supephotphat thu được sau khi làm khô hỗn hợp sau phản ứng là:
Xem thêm đề thi tương tự

40 câu hỏi 1 mã đề 1 giờ
107,463 lượt xem 57,848 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
107,137 lượt xem 57,673 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
103,040 lượt xem 55,468 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
103,663 lượt xem 55,804 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
103,560 lượt xem 55,748 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
102,274 lượt xem 55,055 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
102,781 lượt xem 55,328 lượt làm bài

38 câu hỏi 1 mã đề 1 giờ
101,804 lượt xem 54,803 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
101,026 lượt xem 54,383 lượt làm bài