
Đề thi thử THPT QG môn Hóa học năm 2019
Thời gian làm bài: 1 giờ
Đề thi nằm trong bộ sưu tập: 📘 Tuyển Tập Bộ Đề Thi Ôn Luyện THPT Quốc Gia Môn Hóa Học Các Trường (2018-2025) - Có Đáp Án Chi Tiết 🧪
Hãy bắt đầu chinh phục nào!
Xem trước nội dung:
Giải pháp thực tế và ứng dụng nào sau đây không hợp lý?
Cho 50,0 gam hỗn hợp X gồm Fe3O4, Cu và Mg vào dung dịch HCl loãng dư, sau phản ứng được 2,24 lít H2 (đktc) và còn lại 18,0 gam chất rắn không tan. Phần trăm khối lượng Fe3O4 trong X là:
Dung dịch có môi trường kiềm là:
Ở nhiệt độ cao, lưu huỳnh (dư) oxi hóa được các kim loại nào sau đây về số oxi hóa +3?
Cho các chất đơn chức có công thức phân tử C3H6O2 lần lượt phản ứng với Na, NaOH, NaHCO3. Số phản ứng có thể xảy ra là:
Chia m gam hỗn hợp X gồm Zn, Al, Mg thành 2 phần bằng nhau:
- Phần 1 cho vào dung dịch HCl dư thu được 1,344 lít H2 (đktc).
- Phần 2 nung trong không khí đến khối lượng không đổi thu được 3,04 gam chất rắn.
Giá trị của m là:
Chất nào sau đây không có tính lưỡng tính?
Phát biểu nào sau đây là sai?
Căng da mặt bằng chỉ vàng 24K (Gold thread lift) là một phương pháp thẩm mỹ sử dụng những sợi chỉ vàng gần như tinh khiết 100% có độ dày siêu mảnh 0,1mm để cấy vào da mặt ở tầng sâu của biểu bì, tạo thành một mạng lưới khung đỡ vững chắc, có tác dụng nâng cơ mặt tức thì, giảm nhăn, ngăn ngừa da chảy xệ, giúp trông trẻ trung hơn. Ngoài ra, sự xuất hiện của các sợi lạ dưới da, tạo các “tổn thương giả tạo” giúp tăng sinh collagen và elastine làm cho vùng da trở nên săn chắc hơn. Tính chất vật lí nào sau đây của kim loại giúp vàng có thể kéo thành những sợi chỉ có độ dày siêu mảnh để sử dụng trong phương pháp thẩm mỹ trên?
Thực hiện các thí nghiệm sau:
(a) Cho Na vào H2O.
(b) Cho Ag vào dung dịch H2SO4 loãng.
(c) Cho Zn vào dung dịch HCl.
(d) Cho Cu vào dung dịch AgNO3.
(e) Cho Al vào dung dịch HNO3 đặc, nguội.
Trong các thí nghiệm trên, số thí nghiệm xảy ra phản ứng là:
Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau:
| Mẫu thử | Thuốc thử | Hiện tượng |
| X | Dung dịch NaHCO3 | Có bọt khí |
| X, Y | Dung dịch AgNO3/NH3 | Kết tủa Ag trắng sáng |
| Z | Dung dịch AgNO3/NH3 | Không hiện tượng |
| Y,Z | Cu(OH)2 | Dung dịch xanh lam |
| T | Cu(OH)2 | Dung dịch tím |
Các chất X, Y, Z, T lần lượt là:
Phát biểu nào sau đây không đúng?
Norađrenalin có vai trò quan trọng trong truyền dẫn xung thần kinh. Ađrenalin là hormon tuyến thượng thận có tác dụng làm tăng huyết áp.
.png)
Bậc của amin trong Norađrenalin và Ađrenalin lần lượt là:
Phản ứng điều chế kim loại nào sau đây thuộc phản ứng thủy luyện?
Cho các phát biểu sau:
(a) Các hợp chất hữu cơ nhất thiết phải chứa nguyên tố cacbon và hiđro.
(b) Khi đun chất béo với dung dịch NaOH thị tạo ra sản phẩm hòa tan được Cu(OH)2.
(c) Mỡ bị ôi là do liên kết C=C của gốc axit béo bị oxi hóa chậm bởi oxi không khí.
(d) Xenlulozơ chỉ có cấu tạo mạch không phân nhánh.
(e) Chất béo nhẹ hơn nước nước, không tan trong nước nhưng tan nhiều trong dung môi hữu cơ
không cực.
(f) Cho glyxylalanin vào Cu(OH)2 thấy tạo phức màu tím đặc trưng.
Số phát biểu đúng là:
Xét sơ đồ chuyển hóa: Glyxin + HCl → X; X + NaOH → Y. Y là chất nào sau đây?
Cho x mol bột Fe vào dung dịch chứa y mol FeCl3 và z mol HCl, sau khi kết thúc phản ứng thu được dung dịch X và còn lại t mol kim loại không tan. Biểu thức liên hệ x, y, z, t là:
Cho a gam dung dịch chứa chất X tác dụng vừa đủ với a gam dung dịch chứa chất Y, thu được 2a gam dung dịch chứa một muối Z duy nhất. Cho dung dịch HNO3 loãng dư vào Z, thấy khí không màu thoát ra. Chất X và Y là:
Công thức của polime nào sau đây là phù hợp nhất được sử dụng để sản xuất cái cốc ở hình bên?
.png)
R là kim loại tác dụng được với dung dịch muối Fe(NO3)3, M là kim loại phản ứng được với dung dịch H2SO4 loãng. Hai kim loại R và M theo thứ tự lần lượt là:
Cho quỳ tím lần lượt vào các dung dịch sau: Valin, axit glutamic, glyxin, alanin, lysin. Số dung dịch làm đổi màu quỳ tím là:
Phát biểu nào sau đây là đúng?
Mưa axit tàn phá thảm thực vật, phá hủy các công trình được xây dựng bằng đá, thép. Một trong những khí chủ yếu gây mưa axit là:
Chất nào sau đây là chất điện li yếu?
Cho các phát biểu sau:
(a) Amilopectin trong tinh bột chỉ có các liên kết α-1,4-glicozit.
(b) Ở điều kiện thường, glucozơ và saccarozơ đều là những chất rắn, dễ tan trong nước.
(c) Thủy phân tinh bột thu được fructozơ và glucozơ.
(d) Đa số polime đều tan trong các dung môi thông thường.
(e) Trong công nghiệp dược phẩm, saccarozơ được dùng để pha chế thuốc.
Trong các phát biểu trên, số phát biểu đúng là:
Đốt cháy kim loại X trong oxi thu được oxit Y. Hòa tan Y trong dung dịch HCl loãng dư, thu được dung dịch Z chứa hai muối. Kim loại X là
Khẳng định nào sau đây không đúng?
Ure, (NH2)2CO là một loại phân bón hóa học quan trọng và phổ biến trong nông nghiệp. Ure thuộc loại phân bón hóa học nào sau đây?
Cho 0,1 mol axit α-amino propionic tác dụng vừa đủ với dung dịch HCl, thu được dung dịch X. Cho X tác dụng với 200 ml dung dịch NaOH 1M, thu được dung dịch chứa m gam muối. Giá trị của m là:
Cho 2,24 lit axetilen (đktc) tác dụng với AgNO3 dư trong dung dịch NH3, sau phản ứng hoàn toàn thu được m gam chất rắn. Giá trị của m là:
Phát biểu không đúng là:
Kim loại M phản ứng được với: dung dịch HCl, dung dịch Cu(NO3)2, dung dịch HNO3 (đặc, nguội). Kim loại M là:
Hợp chất hữu cơ X mạch hở có công thức phân tử C7H8O4. Thủy phân hoàn toàn X trong dung dịch NaOH đun nóng, thu được muối Y và hai chất hữu cơ Z và T (thuộc cùng dãy đồng đẳng). Axit hóa Y, thu được hợp chất hữu cơ E (chứa C, H, O). Phát biểu nào sau đây không đúng?
Thực hiện phản ứng este hóa m gam hỗn hợp X gồm etanol và axit axetic (xúc tác: H2SO4 đặc) với hiệu suất phản ứng đạt 80%, thu được 7,04 gam etyl axetat. Mặt khác, cho m gam X tác dụng với NaHCO3 dư, thu được 3,36 lít khí CO2 (ở đktc). Giá trị của m là:
Đốt cháy hoàn toàn 0,1 mol hỗn hợp X chứa trimetylamin và hexametylenđiamin cần dùng 0,715 mol O2, sản phẩm cháy gồm CO2, H2O và N2. Mặt khác cho 24,54 gam X trên tác dụng với dung dịch HCl loãng dư, thu được m gam muối. Giá trị của m là:
Hỗn hợp X chứa chất A (C5H16O3N2) và chất B (C4H12O4N2) tác dụng với dung dịch NaOH vừa đủ, đun nóng cho đến khi phản ứng xảy ra hoàn toàn, rồi cô cạn thu được m gam hỗn hợp Y gồm 2 muối D và E (MD < ME) và 4,48 lít (đktc) hỗn hợp Z gồm 2 amin no, đơn chức, đồng đẳng kế tiếp có tỉ khối so với H2 bằng 18,3. Khối lượng của muối E trong hỗn hợp Y là:
Để hòa tan hết 38,36 gam hỗn hợp R gồm Mg, Fe3O4, Fe(NO3)2 cần 0,87 mol dung dịch H2SO4 loãng, sau khi các phản ứng xảy ra hoàn toàn thu được 111,46 gam sunfat trung hòa và 5,6 lít (đktc) hỗn hợp khí X gồm hai khí không màu, tỉ khối hơi của X so với H2 là 3,8 (biết có một khí không màu hóa nâu ngoài không khí). Phần trăm khối lượng Mg trong R gần với giá trị nào sau đây?
Tiến hành điện phân dung dịch chứa m gam hỗn hợp CuSO4 và KCl. Kết quả quá trình điện phân được biểu diễn trong đồ thị sau:
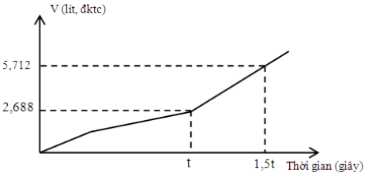
Biết các khí đều đo ở đktc. Giá trị m là:
Cho m gam hỗn hợp A gồm Al và Fe3O4. Nung A trong khí trơ, nhiêt độ cao để phản ứng xảy ra hoàn toàn thu được hỗn hợp B. Nghiền nhỏ B, trộn đều, chia 2 phần không bằng nhau:
Phần 1 (phần ít): Tác dụng với dung dịch NaOH dư thu được 1,176 lít khí H2. Tách riêng chất không tan đem hòa tan trong dung dịch HCl dư thu được 1,008 lít.
Phần 2 (phần nhiều): Cho tác dụng với dung dịch HCl dư thu được 6,552 lít khí.
Giá trị của m và thành phần % khối lượng của một chất có trong hỗn hợp A gần giá trị nào nhất sau
đây? (các thể tích khí đo ở đktc).
Nhỏ từ từ V (lít) dung dịch chứa Ba(OH)2 0,5 M vào dung dịch chứa x mol NaHCO3 và y mol BaCl2. Đồ thị sau đ}y biểu diễn sự phụ thuộc giữa lượng kết tủa và thể tích dung dịch Ba(OH)2 như sau:
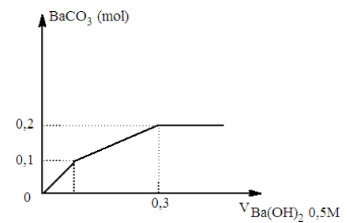
Giá trị của x và y tương ứng là:
Xem thêm đề thi tương tự

40 câu hỏi 1 mã đề 1 giờ
98,930 lượt xem 53,270 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
97,786 lượt xem 52,654 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
111,583 lượt xem 60,081 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
111,827 lượt xem 60,214 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
98,137 lượt xem 52,843 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
98,163 lượt xem 52,857 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
111,983 lượt xem 60,298 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
131,939 lượt xem 71,043 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
131,997 lượt xem 71,071 lượt làm bài

40 câu hỏi 1 mã đề 1 giờ
110,567 lượt xem 59,535 lượt làm bài
