
[2022] Trường THPT Hoàng Diệu - Đề thi thử THPT QG năm 2022 môn Hóa học
Đề thi nằm trong bộ sưu tập: 📘 Tuyển Tập Bộ Đề Thi Ôn Luyện THPT Quốc Gia Môn Hóa Học Các Trường (2018-2025) - Có Đáp Án Chi Tiết 🧪📘 Tuyển Tập Đề Thi Tham Khảo Các Môn THPT Quốc Gia 2025 🎯
Số câu hỏi: 40 câuSố mã đề: 1 đềThời gian: 1 giờ
202,320 lượt xem 15,558 lượt làm bài
Xem trước nội dung:
Trong các nguồn năng lượng: (1) thủy điện, (2) gió, (3) mặt trời, (4) hóa thạch; những nguồn năng lượng sạch là:
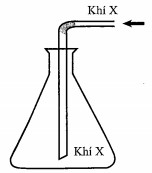
Trong phòng thí nghiệm, khí X được điều chế và thu vào bình tam giác như hình vẽ bên. Khí X được tạo thành từ phản ứng hóa học nào dưới đây?
Thủy phân hoàn toàn 1 mol peptit mạch hở X, thu được 2 mol Gly, 2 mol Ala và 1 mol Val. Mặt khác, thủy phân không hoàn toàn X, thu được hỗn hợp các amino axit và các peptit (trong đó có Gly-Ala-Val). Số công thức cấu tạo phù hợp với tính chất của X là
Phát biểu nào dưới đây sai?
Ma túy đá hay còn gọi là hàng đá, chấm đá là tên gọi chỉ chung cho các loại ma túy tổng hợp, có chứa chất methamphetamine (meth). Những người thường xuyên sử dụng ma túy đá gây hậu quả là suy kiệt thể chất, hoang tưởng, thậm chí mất kiểm soát hành vi, gây hại cho người khác và xã hội, nặng hơn có thể mắc bệnh tâm thần. Khi oxi hóa hoàn toàn 0,5215 gam methamphetamine bằng CuO dư, dẫn sản phẩm cháy lần lượt qua bình (1) đựng H2SO4 đặc, bình (2) đựng Ba(OH)2 dư. Sau khi kết thúc thí nghiệm thấy khối lượng bình (1) tăng 0,4725 gam; ở bình (2) tạo thành 6,895 gam kết tủa và còn 39,2 ml khí (ở đktc) thoát ra. Biết công thức phân tử trùng với công thức đơn giản nhất. Công thức phân tử của methamphetamine là
Thực hiện các thí nghiệm sau:
(1) Đốt dây sắt trong khí clo.
(2) Đốt nóng hỗn hợp Fe và S (trong điều kiện không có oxi).
(3) Cho FeO vào dung dịch HNO3 loãng, dư.
(4) Cho Fe vào dung dịch Fe2(SO4)3.
(5) Cho Fe vào dung dịch H2SO4 loãng dư.
Số thí nghiệm tạo ra muối sắt(II) là
Cho sơ đồ chuyển hóa (mỗi mũi tên ứng với một phản ứng):
Triolein X Y Z
Tên của Z là
Phát biểu nào dưới đây sai?
Cho các chất: NaHCO3, Ca(OH)2, Al(OH)3, SiO2, HF, Cl2, NH4Cl. số chất tác dụng với dung dịch NaOH loãng ở nhiệt độ thường là
Phát biểu nào dưới đây sai?
Cho các phát biểu sau:
(a) Glucozo và saccarozo đều là chất rắn có vị ngọt, dễ tan trong nước.
(b) Tinh bột và xenlulozo đều là polisaccarit.
(c) Trong dung dịch, glucozo và saccarozo đều hòa tan Cu(OH)2 tạo dung dịch màu xanh lam.
(d) Khi thủy phân hoàn toàn hỗn hợp tinh bột và saccarozo trong môi trường axit, chỉ thu được một loại monosaccarit duy nhất.
(e) Khi đun nóng glucozo với dung dịch AgNO3 trong NH3 thu được Ag.
(f) Glucozo và saccarozo đều tác dụng với H2 (Ni, ) tạo sobitol.
Số phát biểu đúng là
Cho dãy chất sau:
p-HO-CH2xC6H4OH; p-HOC6H4COOC2H5;
p-HO C6H4COOH; p-HCOOC6H4 OH; p-CH3OC6H4OH.
Cho các điều kiện sau:
(a) Chỉ tác dụng với NaOH theo tỉ lệ mol 1:1.
(b) Tác dụng với Na dư tạo ra số mol H2 bằng số mol chất phản ứng.
Số chất trong dãy thỏa mãn đồng thời hai điều kiện (a) và (b) là
Phát biểu nào sau đây đúng?
Cho sơ đồ phản ứng sau:
(1) X + O2 → axit cacboxylic Y1
(2) X + H2 → ancol Y2
(3) Y1 + Y2 ⇔ Y3 + H2O
Biết Y3 có công thức phân tử là C6H10O2. Tên gọi của X là
Ancol etylic được điều chế từ tinh bột bằng phương pháp lên men với hiệu suất toàn bộ quá trình là 90%. Hấp thụ hoàn toàn lượng CO2 sinh ra khi lên men vào dung dịch nước vôi trong, thu được 33 gam kết tủa và dung dịch X. Biết khối lượng X giảm đi so với lượng nước vôi trong ban đầu là 13,2 gam. Giá trị của m là
Để trung hòa 20 ml dung dịch HCl 0,1M cần 10 ml dung dịch NaOH nồng độ X mol/l. Giá trị cùa X là
Cho 200 ml dung dịch Ba(OH)2 0,1M vào 300 ml dung dịchNaHCO3 0,1M, thu được dung dịch X và kết tủa Y. Cho từ từ dung dịch HCl 0,25M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của V là
Dung dịch X chứa các ion: và , trong đó số mol của là 0,1. Chia X thành hai phần bằng nhau. Phần một phản ứng với NaOH dư thu được 2 gam kết tủa. Phần hai tác dụng với Ca(OH)2 dư thu được 3 gam kết tủa. Mặt khác, nếu đun sôi đến cạn dung dịch X thu được m gam chất rắn khan. Giá trị của m là
Hỗn hợp khí X gồm O2 và O3 có tỉ khối so với H2 là 22. Hỗn hợp khí Y gồm metylamin và etylamin có tỉ khối so với H2 là 17,833. Để đốt hoàn toàn V1 lít Y cần vừa đủ V2 lít X (biết sản phẩm cháy gồm CO2, H2O và N2, các chất khí đo ở cùng điều kiện nhiệt độ, áp suất). Tỉ lệ V1 : V2 là
Cho các phản ứng xảy ra theo sơ đồ sau:
X + NaOH → Y + Z
Y (rắn) + NaOH (rắn) → CH4 + Na2CO3
Z + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2NH4NO3 + 2Ag
Chất X là
Cho các phát biểu sau:
(a) Khi đốt cháy hoàn toàn anken luôn thu được
(b) Trong thành phần hợp chất hữu cơ nhất thiết phải có cacbon.
(c) Liên kết hóa học chủ yếu trong hợp chất hữu cơ là liên kết cộng hóa trị.
(d) Những hợp chất hữu cơ khác nhau có cùng phân tử khối là đồng phân của nhau.
(e) Phản ứng hữu cơ thường xảy ra nhanh vào không theo một hướng nhất định.
(f) Hợp chất C9H14BrCl có vòng benzen trong phân tử.
Số phát biểu đúng là
Cho các cặp chất với tỉ lệ số mol tương ứng như sau:
(a) Fe3O4 và Cu (1 : 1)
(b) Sn và Zn (2 : 1)
(c) Zn và Cu (1 : 1)
(d) Fe2(SO4)3 và Cu (l : 1)
(e) FeCl2 và Cu (2 : 1)
(g) FeCl3 và Cu (1 : 1)
Số cặp chất tan hoàn toàn trong một lượng dư dung dịch HCl loãng nóng là
Cho 3 hiđrocacbon mạch hở X, Y, Z ( {{M}_{X}}<{{M}_{Y}}<{{M}_{Z}}<62 ) có cùng số nguyên tử cacbon trong phân tử, đều phản ứng với dung dịch AgNO3 trong NH3 dư. Cho các phát biểu sau:
(a) 1 mol chất X phản ứng với 4 mol H2 (Ni, ).
(b) Chất Z có đồng phân hình học.
(c) Chất Y có tên là but-1-in.
(d) Ba chất X, Y, Z đều có mạch cacbon không phân nhánh.
Số phát biểu đúng là
Thực hiện các thí nghiệm sau:
(a) Nung NH4NO3 nóng.
(b) Đun nóng NaCl tinh thể với dung dịch H2SO4 đặc.
(c) Sục khí Cl2 vào dung dịch NaHCO3.
(d) Sục khí CO2 vào dung dịch Ca(OH)2 dư.
(e) Sục khí SO2 vào dung dịch KMnO4.
(f) Cho dung dịch KHSO4 vào dung dịch NaHCO3.
(g) Cho PbS vào dung dịch HCl loãng.
(h) Cho Na2SO3 vào dung dịch H2SO4 dư, đun nóng.
Số thí nghiệm tạo ra chất khí là
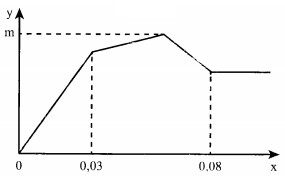
Nhỏ từ từ đến dư dung dịch Ba(OH)2 vào dung dịch gồm Al2(SO4)3 và AlCl3. Sự phụ thuộc của khối lượng kết tủa (y gam) vào so mol Ba(OH)2 (x mol) được biểu diễn bằng đồ thị bên, khối lượng kết tủa cực đại là m gam. Giá trị của m là
Cho 1,82 gam hỗn hợp X gồm Cu và Ag (tỉ lệ mol tương ứng 4 : 1) vào 30 ml dung dịch gồm H2SO4 0,5M và HNO3 2M, sau khi phản ứng xảy ra hoàn toàn, thu được a mol khí NO (sản phẩm khử duy nhất của {{N}^{+5}} ). Trộn a mol NO trên với 0,1 mol O2 thu được hỗn hợp khí Y. Cho toàn bộ Y tác dụng với H2O, thu được 150 ml dung dịch có pH = z. Giá trị của z là
Cho 7,65 gam hỗn hợp X gồm Al và Al2O3 (trong đó Al chiếm 60% khối lượng) tan hoàn toàn trong dung dịch Y gồm H2SO4 và NaNO3, thu được dung dịch Z chỉ chứa ba muối trung hòa và m gam hỗn hợp khí T (trong T có 0,015 mol H2). Cho dung dịch BaCl2 dư vào Z đến khí các phản ứng xảy ra hoàn toàn, thu được 93,2 kết tủa. Còn nếu cho Z phản ứng với NaOH thì lượng NaOH phản ứng tối đa là 0,935 mol. Giá trị của m gần nhất với
Đun hỗn hợp etylen glicol và axit cacboxylic X (phân tử chỉ có nhóm COOH) với xúc tác H2SO4 đặc, thu được hỗn hợp sản phẩm hữu cơ, trong đó có chất hữu cơ Y mạch hở. Đốt cháy hoàn toàn 3,95 gam Y cần 4,00 gam O2, thu được CO2 và H2O theo tỉ lệ mol tương ứng là 2 : 1. Biết Y có công thức phân tử trùng với công thức đơn giản nhất. Y phản ứng với NaOH theo tỉ lệ mol tương ứng 1:2. Phát biểu nào sau đây sai?
Đốt cháy hoàn toàn một este đơn chức, mạch hở X (phân tử có số liên kết π nhỏ hơn 3), thu được thể tích khí CO2 bằng 6/7 thể tích khí O2 đã phản ứng (các thể tích khi đo ở cùng điều kiện). Cho m gam X tác dụng hoàn toàn với 200 ml dung dịch KOH 0,7M thu được dung dịch Y. Cô cạn Y thu được 12,88 gam chất rắn khan. Giá trị của m là
Thực hiện các thí nghiệm sau:
(a) Nhiệt phân AgNO3.
(b) Nung FeS2 trong không khí.
(c) Nhiệt phân KNO3.
(d) Cho dung dịch CuSO4 vào dung dịch NH3 dư.
(e) Cho Fe vào dung dịch CuSO4.
(f) Cho Zn vào dung dịch FeCl3 dư.
(g) Nung Ag2S trong không khí.
(h) Cho Ba vào dung dịch CuSO4 dư.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm sinh ra kim loại là
Hợp chất hữu cơ X (chứa C, H, O) chỉ chứa một loại nhóm chức. Cho 0,15 mol X phản ứng vừa đủ với 180 gam dung dịch NaOH, thu được dung dịch Y. Làm bay hơi Y, chỉ thu được 164,7 gam hơi nước và 44,4 gam hỗn hợp chất rắn khan Z. Đốt cháy hoàn toàn Z, thu được 23,85 gam Na2CO3; 56,1 gam CO2 và 14,85 gam H2O. Mặt khác, Z phản ứng với dung dịch H2SO4 loãng, dư, thu được hai axit cacboxylic đơn chức và hợp chất T (chứa C, H, o và {{M}_{T}}<126 ). Số nguyên tử H trong phân tử T bằng
Hai peptit X, Y ( {{M}_{X}}<{{M}_{Y}} ) mạch hở, có cùng số nguyên tử cacbon, Z là este của amino axit có công thức phân tử C3H7O2N. Đun nóng 47,8 gam hỗn hợp E chứa X, Y, Z cần dùng dung dịch chứa 0,6 mol NaOH, thu được 0,12 mol ancol T và 64,36 gam hỗn hợp muối của glyxin, alanin và valin. Phần trăm khối lượng của Y trong hỗn hợp E là
Chất X có công thức phân tử C6H8O4. Cho 1 mol X phản ứng hết với dung dịch NaOH, thu được chất Y và 2 mol chất Z. Đun Z với dung dịch H2SO4 đặc, thu được đimetyl ete. Chất Y phản ứng với dung dịch H2SO4 loãng, dư, thu được chất T. Cho T phản ứng với HBr, thu được hai sản phẩm là đồng phân cấu tạo của nhau. Phát biểu nào sau đây đúng?
Hòa tan hết 16,58 gam hỗn hợp X gồm Al, Mg, Fe, FeCO3 trong dung dịch chứa 1,16 mol NaHSO4 và 0,24 mol HNO3, thu đuợc dung dịch Z (chỉ chứa muối trung hòa) và 6,89 gam hỗn hợp khí Y gồm CO2, N2, NO, H2 (trong Y có 0,035 mol H2 và tỉ lệ mol NO : N2 = 2 : 1). Dung dịch Z phản ứng tối đa với 1,46 mol NaOH, lọc lấy kết tủa đem nung trong không khí đến khối lượng không đổi, thu được 8,8 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng Fe đơn chất trong X là
Hỗn hợp E gồm chất X ( ) là muối của axit cacboxylic hai chức và chất Y ( ) là muối của axit cacboxylic đơn chức. Đốt cháy hoàn toàn 0,2 mol E cần dùng vừa đủ 0,58 mol O2, thu được N2, CO2 và 0,84 mol H2O. Mặt khác, cho 0,2 mol E tác dụng hết với dung dịch NaOH, cô cạn dung dịch sau phản ứng, thu được một chất khí làm xanh quỳ tím ẩm và m gam hỗn hợp hai muối khan. Giá trị của m là
Hỗn hợp E gồm: X, Y là hai axit đồng đẳng kế tiếp; Z, T là hai este (đều hai chức, mạch hở; Y và Z là đồng phân của nhau; ). Đốt cháy hoàn toàn 12,84 gam E cần vừa đủ 0,37 mol O2, thu được CO2 và H2O. Mặt khác, cho 12,84 gam E phản ứng vừa đủ với 220 ml dung dịch NaOH 1M. Cô cạn dung dịch sau phản ứng, thu được hỗn hợp muối khan G của các axit cacboxylic và 2,8 gam hỗn hợp ba ancol có cùng số mol. Khối lượng muối của axit có phân tử khối lớn nhất trong G là
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho vào ống nghiệm 2-3 giọt CuSO4 5% và 1 ml dung dịch NaOH 10%. Lắc nhẹ, gạn bỏ phần dung dịch. Lấy kết tủa cho vào ống nghiệm (1).
Bước 2: Rót 1,5 ml dung dịch saccarozo 1% vào ống nghiệm (2) và rót tiếp vào đó 0,5 ml dung dịch H2SO4. Đun nóng dung dịch trong 2-3 phút.
Bước 3: Để nguội dung dịch, cho từ từ NaHCO3 tinh thể vào ống nghiệm (2) và khuấy đều bằng đũa thủy tinh cho đến khi ngừng thoát khí CO2.
Bước 4: Rót dung dịch trong ống nghiệm (2) vào ống nghiệm (1), lắc đều cho đến khi kết tủa tan hoàn toàn.
Phát biểu nào sau đây sai?
Câu nào đúng khi nói về lipit?
Chất béo là:
Đề thi tương tự
1 mã đề 40 câu hỏi 1 giờ
218,713 xem16,814 thi
1 mã đề 40 câu hỏi 1 giờ
212,458 xem16,337 thi
1 mã đề 50 câu hỏi 1 giờ
209,836 xem16,127 thi
1 mã đề 40 câu hỏi 1 giờ
206,836 xem15,905 thi
1 mã đề 40 câu hỏi 1 giờ
218,463 xem16,791 thi
1 mã đề 40 câu hỏi 1 giờ
214,209 xem16,468 thi
1 mã đề 50 câu hỏi 1 giờ
210,521 xem16,187 thi
1 mã đề 40 câu hỏi 1 giờ
217,506 xem16,723 thi
1 mã đề 40 câu hỏi 1 giờ
219,521 xem16,881 thi
