
(2025 MỚI NHẤT) Đề Ôn Thi Tốt Nghiệp THPT Môn Hóa Học - Đề Số 9
<p>Cập nhật đề ôn thi tốt nghiệp THPT môn Hóa Học 2025 (Đề số 9) với nội dung bám sát cấu trúc đề thi chính thức của Bộ Giáo dục. Đề thi bao gồm hệ thống câu hỏi lý thuyết quan trọng và bài tập thực hành đa dạng, giúp học sinh củng cố kiến thức, nâng cao kỹ năng và làm quen với các dạng bài thi thực tế. Đây là tài liệu ôn tập cần thiết để bạn tự tin chinh phục kỳ thi tốt nghiệp THPT môn Hóa Học với kết quả cao. Đừng bỏ lỡ tài liệu chất lượng này!</p>
Từ khoá: đề ôn thi tốt nghiệp THPT môn Hóa Họcđề thi thử Hóa Học 2025đề số 9 ôn thi môn Hóa Họctài liệu ôn thi Hóa Học THPTđề thi môn Hóa Học mới nhất 2025luyện thi THPT môn Hóa Học hiệu quảcấu trúc đề thi Hóa Học THPT 2025ôn thi tốt nghiệp THPT môn Hóa Học đạt điểm caođề thi thử môn Hóa Học 2025đề ôn thi môn Hóa Học chất lượng cao
Đề thi nằm trong bộ sưu tập: 📘 Tuyển Tập Đề Thi Tham Khảo Các Môn THPT Quốc Gia 2025 🎯📘 Tuyển Tập Bộ Đề Thi Ôn Luyện THPT Quốc Gia Môn Hóa Học Các Trường (2018-2025) - Có Đáp Án Chi Tiết 🧪
Số câu hỏi: 28 câuSố mã đề: 1 đềThời gian: 1 giờ
224,590 lượt xem 17,271 lượt làm bài
Xem trước nội dung:
Phản ứng refoming là phản ứng làm thay đổi cấu trúc mạch carbon mà không làm thay đổi số nguyên tử carbon của hydrocarbon đó. Trong công nghiệp chế hoá dầu mỏ, người ta thường sử dụng phản ứng refoming để tạo ra các hydrocarbon mạch nhánh hoặc mạch vòng nhằm làm tăng chỉ số octane của xăng. Hãy cho biết phản ứng nào sau đây là phản ứng refoming?
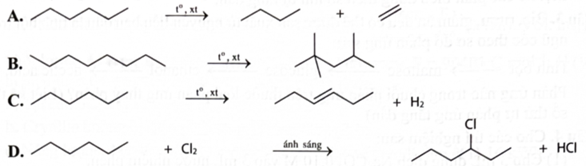
Hình A
Hình B
Hình C
Hình D
Polymer X có cấu tạo như hình bên thuộc loại chất dẻo, trong suốt được dùng để sản xuất kính ô tô, cửa ra vào. Polymer X được tạo ra bằng phản ứng trùng hợp chất nào sau đây?
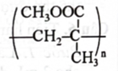
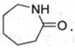
Polymer tổng hợp được tạo ra bằng phản ứng trùng hợp hoặc trùng ngưng. Chất nào sau đây có khả năng tham gia phản ứng trùng ngưng?
 .
.
Trong quá trình luyện gang, ngoài các phản ứng khử để thành Fe còn có một số phản ứng khác theo hai sơ đồ:
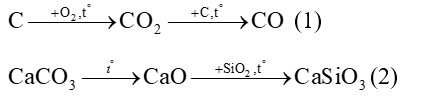
Số phản ứng oxi hoá - khử xảy tra trong hai sơ đồ trên là
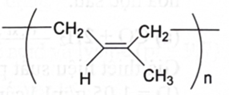
Cao su thiên nhiên được khai thác từ mủ cây cao su. Cao su thiên nhiên có thành phần chính là polymer của isoprene (cấu trúc như hình bên). Cao su thiên nhiên không dẫn điện, không thấm nước và khí, có tính đàn hồi tốt nhưng tính đàn hồi chỉ tồn tại trong một khoảng nhiệt độ hẹp. Phát biểu nào sau đây sai?
Trong môi trường trung tính có quá trình sau:
Cho thế điện cực chuẩn của một số kim loại: , Dựa vào các thông tin trên hãy cho biết kim loại nào sau đây không thể phản ứng với nước ở điều kiện chuẩn.
Một lượng lớn acetic acid được sử dụng để sản xuất vinyl acetate (dùng sản xuất keo dán, chất kết dính trong sản xuất giấy,...) và cellulose acetate (sản xuất tơ, phim ảnh,...). Acetic acid được tổng hợp từ nguồn khí than (giá thành rẻ) theo các phản ứng hoá học sau:
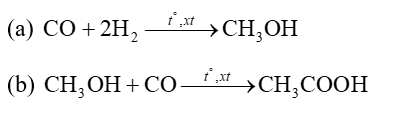
Trong mỗi ý a, b, c, d ở mỗi câu, thí sinh chọn đúng hoặc sai.
Isoamyl acetate có mùi chuối nên được dùng làm hương liệu nhân tạo. Trong ngành sơn, isoamyl acetate được dùng làm dung môi vecni, dung môi sơn mài,... Isoamyl acetate được điều chế theo các bước sau:
Buớc 1. Cho vào bình cầu 15 mL isoamyl alcohol acetic acid và đậm đặc, cho thêm vào bình vài viên đá bọt. Lắp ống sinh hàn hồi lưu thẳng đứng vào miệng bình cầu. Sau đó đun nóng bình cầu trong khoảng 1 giờ.
Buớc 2. Sau khi đun, để nguội rồi rót sản phẩm vào phễu chiết, lắc đều rồi để yên khoảng 5 phút, chất lỏng tách thành hai lớp, loại bỏ phần chất lỏng phía dưới, lấy phần chất lỏng phía trên.
Buớc 3. Cho từ từ dung dịch vào phần chất lỏng thu lấy ở bước 2 và lắc đều cho đến khi không còn khí thoát ra, thêm tiếp 20 mL dung dịch NaCl bão hoà rồi để yên khi đó chất lỏng tách thành hai lớp. Chiết lấy phần chất lỏng phía trên, làm khan, ta thu được isoamyl acetate.
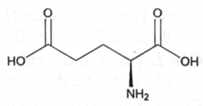
Glutamic acid có vai trò quan trọng trong quá trình xây dựng cấu trúc tế bào của con người. Ngoài ra, muối monosodium glutamate còn được dùng chế biến gia vị thức ăn (bột ngọt hay mì chính). Glutamic acid có cấu trúc như hình bên và có điểm đẳng điện (pI là giá trị pH mà khi đó amino acid có nồng độ ion lưỡng cực là cực đại. Khi thì amino acid đó tồn tại chủ yếu ở dạng cation, còn khi thì amino acid đó tồn tại chủ yếu ở dạng anion).
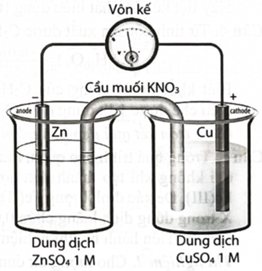
Hai kim loại có , và một pin Galvani được thiết lập như hình vẽ ở
Trong công nghiệp, một lượng lớn và được sản xuất theo phương pháp Solvay bằng cách cho khí (lấy từ nhiệt phân đá vôi) vào dung dịch chứa sodium chloride bão hoà và ammonia bão hoà.
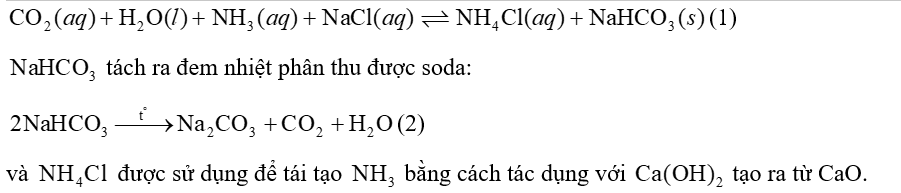
Trong số các chất: có bao nhiêu chất tác dụng được với dung dịch loãng ở nhiệt độ thường?
Trong số các chất: ethyl acetate, tristearin, saccharose, glycerol, glycine, có bao nhiêu chất tác dụng được với dung dịch NaOH khi đun nóng?
Khi nhỏ dung dịch HCl đặc vào dung dịch thấy dung dịch chuyển từ màu xanh sang màu vàng là do xảy ra quá trình:
Cho các phát biểu sau:
(1) Màu dung dịch phức của phụ thuộc vào phối tử.
(2) Phức chất bền hơn phức chất
(3) Màu vàng là màu của ion trong dung dịch.
(4) Cấu trúc của phức là bát diện.
Hãy liệt kê các phát biểu đúng (theo số thứ tự tăng dần).
Từ tinh bột sản xuất được theo sơ đồ sau:
Biết khối lượng riêng của là Khối lượng tinh bột cần thiết để điều chế được 1 lít dung dịch theo sơ đồ trên là bao nhiêu gam?
(Làm tròn kết quả đến hàng đơn vị)
Trong quá trình bảo quản, muối thường bị oxi hoá bởi oxi không khí tạo thành hỗn hợp X chứa các hợp chất của Fe (II) và Để xác định lượng bị oxi hoá người ta hoà tan một lượng X trong dung dịch loãng chứa thu được 100 ml dung dịch Y. Tiến hành hai thí nghiệm với Y:

Thí nghiệm 1. Cho lượng dư dung dịch vào 25 mL dung dịch Y, lọc kết tủa, sấy khô rồi đem cân thu được 4,66 gam chất rắn.
Thí nghiệm 2. Thêm dung dịch (loãng, dư) vào 25 mL dung dịch Y, thu được dung dịch Z. Chuẩn độ dung dịch Z bằng dung dịch chuẩn đến khi đầu xuất hiện màu hồng (tồn tại khoảng 20 giây) thì hết
Phần trăm Fe (II) đã bị oxi hoá trong không khí bằng bao nhiêu?
(Làm tròn kết quả đến hàng phần mười)
Acetylsalicylic acid được dùng làm thuốc cảm aspirin. Acetylsalicylic acid được điều chế theo phản ứng sau:
Salicylic acid Anhydride acetic Acetylsalicylic acid
Biết mỗi vỉ thuốc aspirin có 10 viên (mỗi viên chứa 500 mg acetylsalicylic acid) và hiệu suất phản ứng tính theo salicylic acid là 92 %. Để sản xuất 3 triệu vỉ thuốc cảm aspirin cần tối thiểu bao nhiêu tấn salicylic acid?
(Làm tròn kết quả đến hàng phần mười)
Đề thi tương tự
1 mã đề 28 câu hỏi 1 giờ
305,803 xem23,515 thi
1 mã đề 28 câu hỏi 1 giờ
290,846 xem22,367 thi
1 mã đề 28 câu hỏi 1 giờ
318,603 xem24,502 thi
1 mã đề 28 câu hỏi 1 giờ
278,059 xem21,383 thi
1 mã đề 28 câu hỏi 1 giờ
289,789 xem22,283 thi
1 mã đề 28 câu hỏi 1 giờ
308,470 xem23,723 thi
1 mã đề 28 câu hỏi 1 giờ
231,755 xem17,820 thi
1 mã đề 28 câu hỏi 1 giờ
228,781 xem17,592 thi
1 mã đề 28 câu hỏi 1 giờ
271,924 xem20,912 thi
