
Trắc nghiệm tổng hợp ôn thi tốt nghiệp THPT môn Hóa Bài 10. Thế điện cực chuẩn của kim loại có đáp án
Từ khoá: grade_thptqg subject_chemistry topic_specific practice_exams detailed_solutions test_prep chemistry_questions national_exam problem_solving electrochemistry_topic
Đề thi nằm trong bộ sưu tập: 📘 Tuyển Tập Bộ Đề Thi Ôn Luyện THPT Quốc Gia Môn Hóa Học Các Trường (2018-2025) - Có Đáp Án Chi Tiết 🧪📘 Tuyển Tập Đề Thi Tham Khảo Các Môn THPT Quốc Gia 2025 🎯
Số câu hỏi: 32 câuSố mã đề: 1 đềThời gian: 1 giờ
290,326 lượt xem 22,326 lượt làm bài
Xem trước nội dung:
Cho hai phản ứng sau:
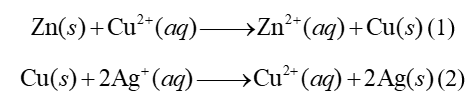
Số cặp oxi hoá - khử trong hai phản ứng trên là
Cho phản ứng oxi hoá - khử sau: Dựa vào phản ứng đã cho, hãy cho biết phát biểu nào sau đây đúng.
Thế điện cực chuẩn của cặp oxi hoá - khử càng lớn thì tính oxi hoá của...(1)... càng mạnh và tính khử của...(2)... càng yếu. Thông tin phù hợp điền vào (1) và (2) lần lượt là
Cho biết: Cho các phản ứng sau:
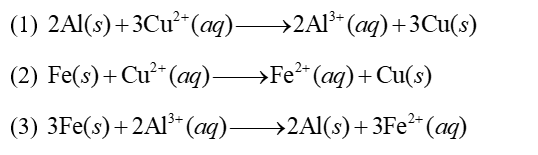
Ở điều kiện chuẩn, phương trình hoá học nào sau đây đúng?
Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá - khử sau:
| Cặp oxi hoá -khử |
|
|
|
|
|
|
|
|
|
| 0 | 0,340 |
Số kim loại trong dãy các kim loại phản ứng được với dung dịch HCl ở điều kiện chuẩn là
Cho biết giá trị thế điện cực chuẩn của các cặ̣p oxi hoá - khử sau:
| Cặp oxi hoá - khử |
|
|
|
|
|
|
|
|
| 0,340 | 0,771 | 0,799 |
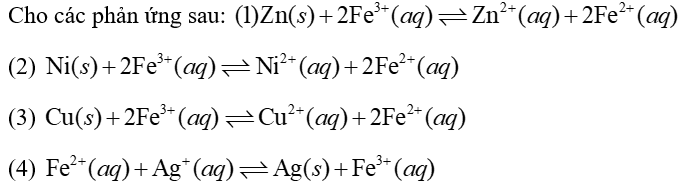
Ở điều kiện chuẩn, số phản ứng hoá học xảy ra theo chiều thuận là
Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá - khử sau:
| Cặp oxi hoá - khử |
|
|
|
|
|
|
|
|
| 0 | 0,340 | 0,771 |
Hãy cho biết đồng có thể bị hoà tan trong dung dịch nào sau đây.
Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá - khử sau:
| Cặp oxi hoá - khử |
|
|
|
|
|
|
|
|
|
|
|
| 0,340 | 0,771 |
Kim loại nào sau đây khi lấy dư chỉ khử được trong dung dịch thành ?
Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá - khử sau:
| Cặp oxi hoá - khử |
|
|
|
|
|
|
|
|
|
|
|
|
Số kim loại trong dãy gồm: và Ni có thể khử được ion tạo ra ở điều kiện chuẩn là
Ở điều kiện chuẩn xảy ra các phản ứng sau:
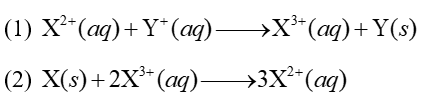
Sự sắp xếp nào sau đây đúng với các giá trị thế điện cực chuẩn của các cặp oxi hoá - khử?
Trong mỗi ý a, b, c, d ở mỗi câu, hãy chọn đúng hoặc sai.
Mỗi phát biểu sau là đúng hay sai?
Quá trình chuyển từ dạng oxi hoá sang dạng khử của cặp oxi hoá - khử được gọi là quá trình khử.
Dạng oxi hoá và dạng khử của cùng một nguyên tố kim loại M : tạo nên cặp oxi hoá - khử và kí hiệu là
Trong một cặp oxi hoá - khử, dạng oxi hoá và dạng khử không phản ứng với nhau.
Trong cặp oxi hoá - khử, tính oxi hoá của dạng oxi hoá luôn mạnh hơn tính oxi hoá của dạng khử.
Nhúng thanh kim loại X và thanh kim loại Y (cùng hoá trị II) vào các dung dịch muối sulfate nồng độ 1 M của chúng ở Quá trình thí nghiệm được mô tả bởi hình vẽ sau:
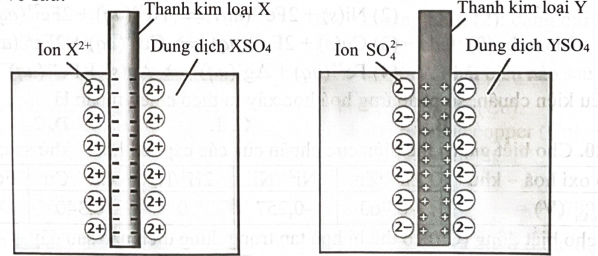
Mỗi phát biểu sau là đúng hay sai?
Bề mặt thanh kim loại X mang điện tích âm và bề mặt thanh kim loại Y mang điện tích dương.
Giữa bề mặt thanh kim loại và dung dịch muối tồn tại cân bằng giữa dạng oxi hoá và dạng khử.
Tính khử của kim loại Y mạnh hơn tính khử của kim loại X.
Khi nối hai thanh kim loại với nhau bằng dây dẫn và nối hai dung dịch muối với nhau bằng cầu muối, sẽ xuất hiện một dòng điện trên dây dẫn.
Cho biết: Mỗi phát biểu sau là đúng hay sai?
Tính khử của kim loại Na mạnh hơn tính khử của kim loại Cu.
Tính oxi hoá của ion mạnh hơn tính oxi hoá của ion
Trong dung dịch, kim loại Na khử được ion thành kim loại Cu.
Trong dung dịch, kim loại Cu khử được ion thành kim loại Na.
Trong mỗi ý a, b, c, d ở mỗi câu, hãy chọn đúng hoặc sai.
Trong cặp oxi hoá - khử, các nguyên tử trong dạng oxi hoá có số oxi hoá khác với các nguyên tử trong dạng khử.
Các kim loại có tính khử mạnh hơn sẽ khử được các cation của kim loại yếu hơn trong dung dịch muối.
Trong dãy điện hoá, các cặp oxi hoá - khử được sắp xếp theo chiều tăng dần giá trị thế điện cực chuẩn.
Mỗi phản ứng oxi hoá - khử đều có lớn hơn một cặp oxi hoá - khử.
Cho dãy các kim loại và ion sau: Có bao nhiêu cặp oxi hoá - khử có thể tạo từ các kim loại và ion đó?
Cho phản ứng oxi hoá - khử: Có bao nhiêu cặp oxi hoá - khử trong phản ứng đó?
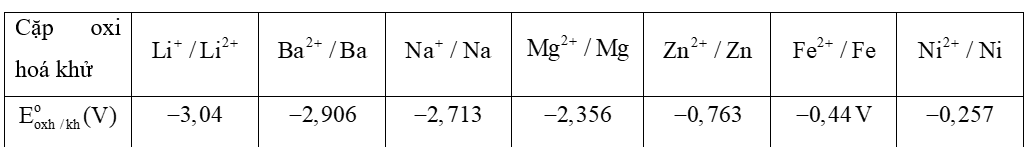
Trong các kim loại , có bao nhiêu kim loại có tính khử mạnh hơn kẽm ?
Cho các kim loại sau: Ở điều kiện chuẩn, có bao nhiêu kim loại trong dãy khử được ion trong dung dịch thành khí ?


Đề thi tương tự
10 mã đề 149 câu hỏi 1 giờ
184,74614,203
1 mã đề 30 câu hỏi 1 giờ
337,63025,960
1 mã đề 57 câu hỏi 1 giờ
292,20722,472
7 mã đề 113 câu hỏi 1 giờ
158,00112,147
6 mã đề 165 câu hỏi 1 giờ
177,45113,642
1 mã đề 28 câu hỏi 1 giờ
291,72122,430
1 mã đề 66 câu hỏi 1 giờ
305,88923,526
1 mã đề 20 câu hỏi 1 giờ
318,56824,500
4 mã đề 49 câu hỏi 1 giờ
160,55312,344
1 mã đề 28 câu hỏi 1 giờ
305,92023,526
