
Trắc nghiệm tổng hợp ôn thi tốt nghiệp THPT môn Hóa Bài 11. Nguồn điện hóa học có đáp án
Từ khoá: grade_thptqg subject_chemistry topic_specific practice_exams detailed_solutions chemistry_questions national_exam test_prep problem_solving electrochemistry_topic
Đề thi nằm trong bộ sưu tập: 📘 Tuyển Tập Bộ Đề Thi Ôn Luyện THPT Quốc Gia Môn Hóa Học Các Trường (2018-2025) - Có Đáp Án Chi Tiết 🧪📘 Tuyển Tập Đề Thi Tham Khảo Các Môn THPT Quốc Gia 2025 🎯
Số câu hỏi: 59 câuSố mã đề: 1 đềThời gian: 1 giờ
292,008 lượt xem 22,458 lượt làm bài
Xem trước nội dung:
Cho các phản ứng hoá học sau:
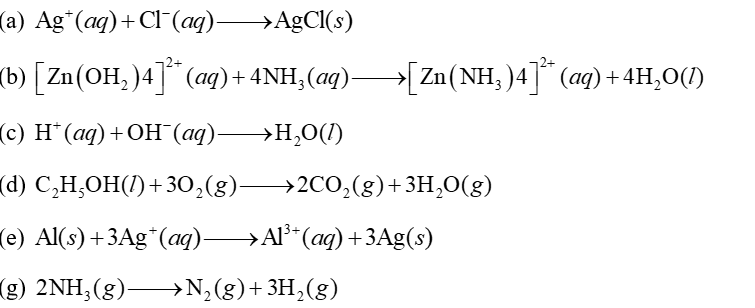
Số phản ứng có thể chuyển hoá năng lượng phản ứng thành điện năng thông qua việc lập các pin điện hoá là
A. 5.
Trong pin Galvani X-Y có phản ứng chung là:
Quá trình xảy ra tại cathode (hay cực dương) của pin là
Cho biết sức điện động chuẩn của các pin sau:
| Pin điện hoá | X-Y | M-Y | M-Z |
| Sức điện động chuẩn (V) | 0,20 | 0,60 | 0,30 |
Sự sắp xếp nào sau đây đúng với tính khử của các kim loại ?
Cho biết thế điện cực chuẩn của các cặp oxi hoá - khử sau:
| Cặp oxi hoá - khử |
|
|
|
|
|
|
|
|
| 0,340 | 0,799 | 0,854 |
Một trong số các pin trên có sức điện động chuẩn là Pin nào sau đây ứng với giá trị đó?
Cho thế điện cực chuẩn của một số kim loại như sau:
| Cặp oxi hoá – khử |
|
|
|
|
|
|
|
|
|
| 0,340 | 0,854 |
Kết luận nào sau đây là không đúng?
Pin quả chanh được thiếp lập gồm một dây Cu và dây Zn ghim vào một quả chanh và nối với bóng điện như hình bên. Bóng điện sáng đồng nghĩa với sự xuất hiện dòng điện. Bán phản ứng nào sau đây xảy ra ở cực dương?

Phản ứng xảy ra khi sạc của một pin Li-ion là:
Để có được một pin điện có dung lượng là 4000 mAh thì khối lượng tối thiểu trước khi sạc là bao nhiêu?
Cho biết: điện lượng là 96485 C và A.s.
Phản ứng của acquy chì khi sạc điện là:
Chất được sinh ra ở cực âm khi acquy chì sạc điện là
Phản ứng của acquy chì khi xả điện là:
Khi đó, Pb sẽ bị oxi hoá và tạo thành bám vào điện cực và bị khử thành bám vào điện cực. Phát biểu nào sau đây đúng trong quá trình acquy xả điện?
Pin nhiên liệu đang được đặc biệt quan tâm nghiên cứu vì tiềm năng sử dụng trong tương lai do có nhiều ưu điểm so với pin Galvani hiện nay. Dòng điện tạo ra trong pin do phản ứng oxi hoá nhiên liệu bằng của không khí. Ưu điểm của pin là sản sinh dòng điện với hiệu suất cao.
Cấu tạo và cơ chế hoạt động của pin nhiên liệu hydrogen như sau:
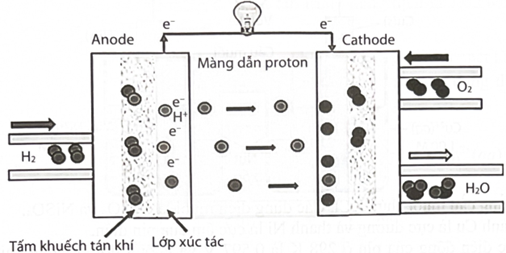
Phản ứng chung trong pin nhiên liệu hydrogen là
Trong mỗi ý a, b, c, d ở mỗi câu, hãy chọn đúng hoặc sai.
Cho cấu tạo của pin Galvani như hình dưới.
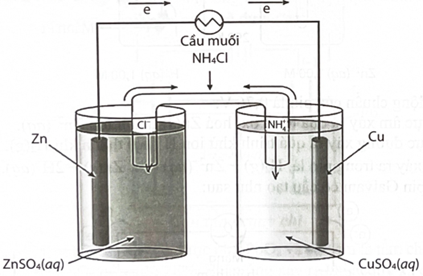
a. Thanh Zn là cực âm (anode) và thanh Cu là cực dương (cathode).
b. Phản ứng xảy ra trong pin là:
c. Khi hoặc hết thì phản ứng trong pin sẽ ngừng lại.
d. Sức điện động của pin không thay đổi cho đến khi phản ứng trong pin xảy ra hoàn toàn.
Cho biết: Một pin điện có cấu tạo như hình sau.
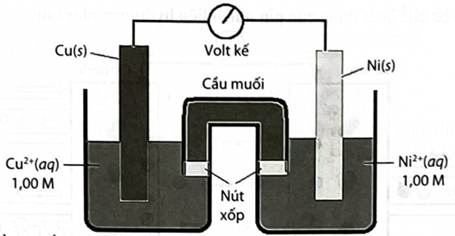
Biết rằng cầu muối chứa KCl. Các dung dịch muối là và
a. Thanh Cu là cực dương và thanh Ni là cực âm của pin điện.
b. Sức điện động của pin ở 298 K là và không đổi cho đến khi pin ngừng hoạt động.
c. Cầu muối KCl có tác dụng trung hoà điện tích của hai dung dịch muối.
d. Khối lượng điện cực Ni và Cu không thay đổi trong quá trình pin hoạt động.
Cho pin điện hoá có cấu tạo như sau:
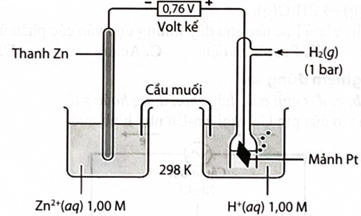
Một pin Galvani có cấu tạo như sau:
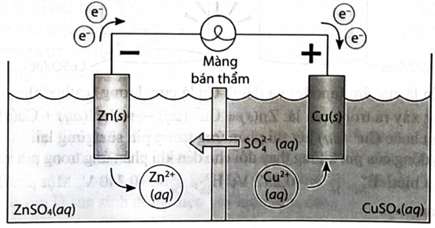
Trong đó, màng bán thẩm chỉ cho nước và các anion đi qua. Biết rằng thể tích của các dung dịch đều là và nồng độ chất tan trong dung dịch là Cho biết:
a. Khối lượng điện cực zinc giảm đúng bằng khối lượng điện cực copper tăng.
b. Nồng độ ion trong dung dịch tăng và trong dung dịch giảm dần.
c. Sức điện động chuẩn của pin là
d. Phản ứng chung xảy ra trong pin điện là
Tiến hành thí nghiệm như hình vẽ dưới đây:
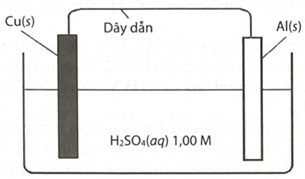
Mỗi phát biểu sau là đúng hay sai?
a. Tại thanh nhôm xảy ra quá trình oxi hoá Al thành cation và tan vào nước.
b. Các electron chuyền từ thanh nhôm sang thanh đồng qua dây dẫn.
d. Nồng độ trong dung dịch không thay đổi trong quá trình thí nghiệm.
Acquy chì có cấu tạo như hình vẽ dưới đây:
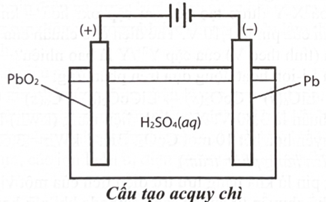
Cực dương là thanh than chì được phủ và cực âm là tấm chì , cùng nhúng vào dung dịch nồng độ . Phản ứng xảy ra khi acquy xả điện là:
Biết rằng sinh ra từ điện cực nào đều bám hết vào điện cực đó.
a. Tại anode, Pb bị khử và tạo thành
b. Tại cathode, bị oxi hoá và tạo thành
c. Khi acquy xả điện, khối lượng các điện cực tăng lên.
d. Nồng độ trong acquy chì giảm xuống khi acquy xả điện.
Mỗi phát biểu sau là đúng hay sai?
a. Trong các pin điện hoá, tại cực âm xảy ra quá trình oxi hoá.
b. Các pin nhiên liệu hoạt động dựa trên các phản ứng oxi hoá hoàn toàn các nhiên liệu.
c. Phản ứng trong các pin nhiên liệu methanol-oxygen là phản ứng oxi hoá methanol bởi khí O2 thành fomaldehyde.
d. Các acquy được sạc lại bằng cách nối cùng cực (âm với âm, dương với dương) của dòng điện một chiều.
Cho biết: Một pin điện hoá được tạo bởi hai cặp oxi hoá - khử là và Sức điện động chuẩn của pin là bao nhiêu milivolt ?
Pin có sức điện động chuẩn là với hai cặp oxi hoá - khử là và Pin có sức điện động chuẩn là với hai cặp oxi hoá - khử là và Pin (với hai cặp oxi hoá - khử là và ) có sức điện động chuẩn là bao nhiêu volt ?
Điện lượng (q) là một đại lượng đặc trưng cho lượng electron mà các điện cực trao đổi trong pin điện. Khi đó, điện lượng được xác định bởi biểu thức sau:
số mol electron (F là 1 mol điện lượng, ).
Một pin điện hoá được cấu tạo như sau:
Thanh kẽm nhúng vào 100 mL dung dịch
Thanh đồng nhúng vào 100 mL dung dịch
Hai thanh kim loại được nối bằng dây dẫn với một thiết bị tiêu thụ điện và hai dung dịch nối với nhau bằng cầu muối. Phản ứng dừng lại khi trong dung dịch bị khử hết thành Cu. Điện lượng (tính theo C) mà pin đó đã sản sinh là bao nhiêu?
(Làm tròn kết quả đến hàng đơn vị)
Pin điện hoá được tạo bởi hai cặp oxi hoá - khử là và Sức điện động chuẩn của pin là Thế điện cực chuẩn của cặp là Thế điện cực chuẩn (tính theo V) của cặp là bao nhiêu?
Một loại pin Li-ion hoạt động dựa trên phản ứng:
có sức điện động chuẩn là Xác định điện năng lớn nhất mà pin đó có thể sản sinh khi chuyển hoá hết Biết
(Làm tròn kết quả đến hàng phần trăm)
Dung lượng pin là khả năng lưu trữ điện tích của một viên pin, được xác định bởi điện lượng có thể chuyển từ anode sang cathode khi pin hoạt động. Một viên pin có dung lượng 4000 mAh thì số mmol electron có thể chuyển từ anode sang cathode là bao nhiêu? (Làm tròn kết quả đến hàng đơn vị)
Cho biết: electron có điện lượng là 96485 C.
Một máy điện sử dụng các pin nhiên liệu để phát điện với nguyên liệu là khí hydrogen và có hiệu suất điện là 56 % (nghĩa là có 56 % năng lượng của phản ứng chuyển hoá thành điện năng). Mỗi ngày nhà máy sản xuất được 500 kWh. Tính khối lượng (theo kg) khí hydrogen tiêu thụ? (Làm tròn kết quả đến hàng phần mười)
Cho biết:
Cho phản ứng:
Nhà máy phát điện sử dụng pin nhiên liệu methane với hiệu suất điện là (nghĩa là có năng lượng của phản ứng chuyển hoá thành điện năng). Nếu một khu dân cư tiêu thụ 10000 kWh mỗi ngày và sử dụng khí methane để phát điện thì khối lượng methane tiêu thụ hàng ngày là bao nhiêu kg? (Làm tròn kết quả đến hàng đơn vị) Cho biết:
Đề thi tương tự
10 mã đề 149 câu hỏi 1 giờ
184,813 xem14,203 thi
1 mã đề 30 câu hỏi 1 giờ
337,656 xem25,960 thi
1 mã đề 57 câu hỏi 1 giờ
292,236 xem22,472 thi
7 mã đề 113 câu hỏi 1 giờ
158,052 xem12,147 thi
6 mã đề 165 câu hỏi 1 giờ
177,465 xem13,642 thi
1 mã đề 28 câu hỏi 1 giờ
291,766 xem22,430 thi
1 mã đề 66 câu hỏi 1 giờ
305,938 xem23,526 thi
1 mã đề 20 câu hỏi 1 giờ
318,591 xem24,500 thi
4 mã đề 49 câu hỏi 1 giờ
160,573 xem12,344 thi
1 mã đề 28 câu hỏi 1 giờ
305,946 xem23,526 thi
